
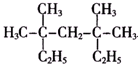
 3,3,5,5-四甲基庚烷.
3,3,5,5-四甲基庚烷.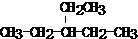 .
.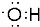 .
.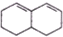 与Br2发生1,4-加成反应的化学方程式为
与Br2发生1,4-加成反应的化学方程式为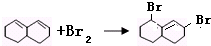 .
.分析 (1)烷烃命名时,应选最长的碳链为主链,从离支链近的一端开始编号;
(2)根据支链的长度不能超过其所在位置两侧的主链的长度来分析;
(3)羟基不显电性,没有得到或失去的电子;
(4) 与Br2发生1,4-加成生成
与Br2发生1,4-加成生成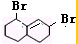 ,据此写出反应的化学方程式;
,据此写出反应的化学方程式;
(5)a.实验室制乙烯时,需要测定反应液温度,必须将温度计的水银球插入反应液中;
b.溴乙烷为非电解质,氯乙烷溶于AgNO3的HNO3溶液中不会发生反应;
c.溶液中挥发出的乙醇也能被酸性高锰酸钾溶液氧化;
d.铜丝在酒精灯上加热变黑后,生成CuO,CuO与乙醇反应生成乙醛、Cu、水;
(6)C2H4Br2的结构简式有两种:BrCH2CH2Br、CH3CHBr2,核磁共振氢谱中峰值数等于有机物中氢原子的种类数,核磁共振氢谱中只给出一种峰,说明该分子中只有1种H原子,据此判断A、B的结构简式及B的核磁共振氢谱中吸收峰的数目.
解答 解:(1)烷烃命名时,应选最长的碳链为主链,故主链上有7个碳原子,即庚烷,从离支链近的一端开始编号,则在3号碳和5号碳上分别均有2个甲基,故名称为:3,3,5,5-四甲基庚烷,
故答案为:3,3,5,5-四甲基庚烷;
(2)烷烃中含有乙基,则乙基至少在3号位,所以只有一个乙基且式量最小的烷烃的结构简式为: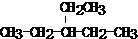 ,
,
故答案为: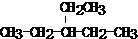 ;
;
(3)氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子,电子式为: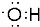 ,
,
故答案为: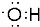 ;
;
(4) 与Br2发生1,4-加成生成
与Br2发生1,4-加成生成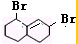 ,反应的化学方程式为:
,反应的化学方程式为: ,
,
故答案为: ;
;
(5)a.实验室制乙烯时,需要测定反应液温度,所以将温度计的水银球插入液面以下,故a正确;
b.溴乙烷为非电解质,不能电离出氯离子,则氯乙烷溶于AgNO3的HNO3溶液中不会发生反应,故b错误;
c.溴乙烷消去反应是在氢氧化钠的乙醇溶液中进行,溶液中挥发出的乙醇也能被酸性高锰酸钾溶液氧化,所以应该利用溴水检验乙烯,故c错误;
d.铜丝在酒精灯上加热变黑后,生成CuO,CuO与乙醇反应生成乙醛、Cu、水,铜丝会恢复成原来的红色,故d正确;
故答案为:bc;
(6)分子式为C2H4Br2的结构简式有两种:BrCH2CH2Br、CH3CHBr2,
A的核磁共振氢谱中只给出一种峰,说明该分子中只有1种H原子,则A的结构简式为:BrCH2CH2Br,
所以B的结构简式为:CH3CHBr2,B分子中含有两种H原子,所以核磁共振氢谱上有2个峰,
故答案为:BrCH2CH2Br;2.
点评 本题考查了有机物结构与性质,题目难度中等,注意熟练掌握常见有机物结构与性质,明确羟基和氢氧根电子式的区别,试题培养了学生的分析能力及灵活应用基础知识的能力.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:选择题
| R | T | |
| X | Y | Z |
| A. | R位于元素周期表中第二周期第ⅣA族 | |
| B. | 原子半径:X<R<T | |
| C. | 最简单气态氢化物稳定性:T>R>Y | |
| D. | 最高价氧化物的水化物酸性:T>R>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在:K+、Na+、AlO2-、SO42- | |
| B. | 向1 mo1•L-l CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | |
| C. | 25℃时,将a mo1•L-l氨水与0.01 moI•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| D. | 已知298K时,MgCO3的Ksp=6.82×10-6,溶液中c(Mg2+)=0.0001 mol•L-1,c(CO32-)=0.0001 mol•L-1,此时Mg2+和CO32-不能共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
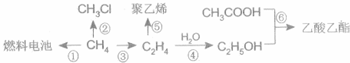
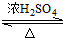 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在地壳中,C元素的含量位于第一位 | |
| B. | 由B、C、D三种元素组成的盐只有两种 | |
| C. | C元素位于元素周期表中的第3周期第ⅠA族 | |
| D. | B元素与氢元素形成化合物的化学式一定为H2B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com