
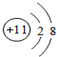 ,写出Cl在周期表中的位置第三周期VIIA族.
,写出Cl在周期表中的位置第三周期VIIA族.分析 (1)钠原子核外有11个电子,最外层一个电子,属于活泼金属,易失去最外层的一个电子形成带一个正电荷的钠离子,氯原子核外有17个电子,核电荷数为17,原子核外三个电子层,最外层七个电子,位于周期表中的第三周期,ⅤⅡA族;
(2)84-消毒液其中含有强氧化性物质次氯酸钠(NaClO),属于强碱弱酸盐,溶液中次氯酸根离子水解显碱性,84-消毒液的PH一般为10.2左右,PH试纸只能粗略测定溶液PH得到整数值,所以选择精密仪器测定;
(3)氯化钠和水在通电条件下生成氢氧化钠、氢气和氯气,氯气与阴极生成的氢氧化钠溶液反应是次氯酸、氯化钠和水,制得有较强杀菌能力的消毒液(NaClO),合并书写得到电解精制饱和食盐水制得NaClO的化学方程式.
解答 解:(1)钠原子核外有11个电子最外层一个电子,属于活泼金属,易失去最外层的一个电子形成带一个正电荷的钠离子,离子的结构示意图为: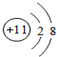 ,氯原子核外有17个电子,核电荷数为17,原子核外三个电子层,最外层七个电子,电子层数=周期序数,最外层电子数=主族族序数,氯元素位于周期表中的第三周期,ⅤⅡA族,
,氯原子核外有17个电子,核电荷数为17,原子核外三个电子层,最外层七个电子,电子层数=周期序数,最外层电子数=主族族序数,氯元素位于周期表中的第三周期,ⅤⅡA族,
故答案为: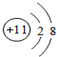 ,第三周期第,ⅤⅡA族;
,第三周期第,ⅤⅡA族;
(2)84-消毒液其中含有强氧化性物质次氯酸钠(NaClO),属于强碱弱酸盐,溶液中次氯酸根离子水解,溶液显碱性,ClO-+H2O?HClO+OH-,84-消毒液的PH一般为10.2左右,PH试纸只能粗略测定溶液PH得到整数值,所以选择精密仪器测定,选择PH计,
故答案为:碱性,PH计;
(3)氯化钠和水在通电条件下生成氢氧化钠、氢气和氯气,2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,氯气与阴极生成的氢氧化钠溶液反应生成次氯酸、氯化钠和水,制得有较强杀菌能力的消毒液(NaClO),制取消毒液所涉及反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,工业上可用电解精制饱和食盐水制得NaClO,电解时发生反应的化学方程式可以表示为:NaCl+H2O $\frac{\underline{\;通电\;}}{\;}$ NaClO+H2↑,
故答案为:NaCl+H2O $\frac{\underline{\;通电\;}}{\;}$ NaClO+H2↑.
点评 本题考查了微粒结构分析,盐类水解原理的理解应用,溶液PH测定和电解原理的分析判断,主要是微粒结构和电解反应的书写,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中CuO和C高温反应的气体产物: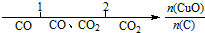 | |
| B. | Na2O2和等物质的量的CO2、H2O(g):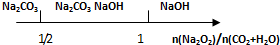 | |
| C. | NaOH溶液中通入一定量的CO2的产物: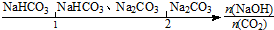 | |
| D. | AlCl3溶液中滴加NaOH溶液后体系中铝元素的存在形式: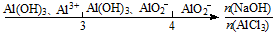 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发酵粉的主要成分为碳酸钠 | |
| B. | 在饱和的碳酸钠溶液中通入二氧化碳,会产生沉淀 | |
| C. | 与盐酸反应的激烈程度:碳酸钠大于碳酸氢钠 | |
| D. | 等质量的碳酸钠和碳酸氢钠与足量的盐酸反应,碳酸钠产生的氢气多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由上述反应可知,Fe(OH)3的氧化性强于FeO42- | |
| B. | 高铁酸钾中铁显+6价 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为3:2 | |
| D. | K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0mol•L-1KNO3溶液:H+、Fe2+、SCN-、SO42- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的溶液:S2-、NO3-、Cl-、Na+ | |
| C. | 0.1 mol•L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | |
| D. | 由水电离出来的c(H+)=10-10mol•L-1的溶液:Na+、SO42-、S2-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,5-二甲基己烷 | B. | 2,3-二甲基丁烷 | ||
| C. | 2,3,4-三甲基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,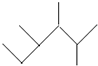 的名称为2,3-二甲基-4-乙基庚烷 的名称为2,3-二甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 | |
| C. | 石油裂解可以得到乙烯,煤液化可得到煤焦油、粗氨水、粗苯等液体 | |
| D. | 1molHC≡CCHO最多能与3mol H2完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 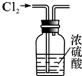 干燥Cl2 | B. | 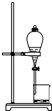 分离汽油与食盐溶液 | ||
| C. | 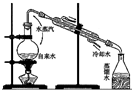 实验室制取少量蒸馏水 | D. | 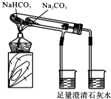 比较Na2CO3与NaHCO3的稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸的物质的量浓度是0.5mol•L-1 | B. | 氢氧化钠溶液的体积是250mL | ||
| C. | 铁和硅的物质的量之比为2:1 | D. | 铁和硅的质量之比为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com