
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| BaSO4(BaCO3) | ||
| FeSO4(CuSO4) | ||
| NaCl(HCl) |
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| BaSO4(BaCO3) | HCl | BaCO3+2H+=Ba2++H2O+CO2↑ |
| FeSO4(CuSO4) | Fe | Fe+Cu2+=Fe2++Cu |
| NaCl(HCl) | NaOH | H++OH-=H2O |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
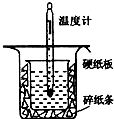 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于右图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于右图所示的装置中进行中和热的测定实验,回答下列问题:| 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
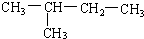 (9)CH2=CH-CH3(8)
(9)CH2=CH-CH3(8)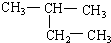 (10)
(10) (11)2,2-二甲基丁烷
(11)2,2-二甲基丁烷查看答案和解析>>
科目:高中化学 来源: 题型:
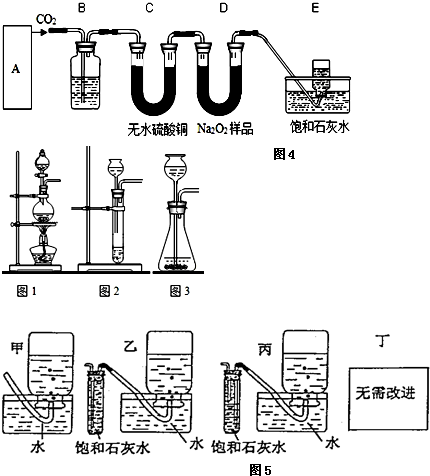
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com