
| A. | 用10mL量筒量取6.8mL稀H2SO4 | |
| B. | 用碱式滴定管量取15.80mLKMnO4溶液 | |
| C. | 酸碱中和滴定时,滴定管需用标准液或待测液润洗 | |
| D. | 中和热测定时,氢氧化钠溶液稍过量的目的是为了保证盐酸完全被中和 |
分析 A、量筒能精确到0.1mL;
B、强氧化性溶液只能盛放到酸式滴定管中;
C、滴定管要用所盛放的溶液来润洗;
D、为了保证酸碱之间完全中和,往往需要一方过量.
解答 解:A、量筒能精确到0.1mL,故可以用10mL量筒量取6.8mL稀H2SO4,故A正确;
B、强氧化性溶液只能盛放到酸式滴定管中,盛放到碱式滴定管中会造成橡胶管的腐蚀,故B错误;
C、滴定管要用所盛放的溶液来润洗,否则所盛放的溶液会造成稀释,故C正确;
D、为了保证酸碱之间完全中和,往往需要一方过量,实验中氢氧化钠溶液稍过量是为了使盐酸完全被氢氧化钠中和,故D正确.
故选B.
点评 本题考查了滴定管的使用以及中和热的测定,中和热指的是强酸和强碱的稀溶液发生中和反应生成1mol水释放的热量,是一个定值,这是解题的关键,难度不大.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:解答题
| 危险性 | 危险品 |
| 储运要求 | 远离金属粉末、氨、烃类、醇等物质,设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
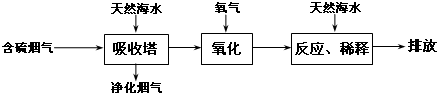
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol双氢青蒿素的质量为284g?mol-1 | |
| B. | 双氢青蒿素的摩尔质量等于它的相对分子质量 | |
| C. | 14.2g双氢青蒿素中含有的原子总数为2.2NA | |
| D. | 含有6.02×1023个碳原子的双氢青蒿素的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCl2溶液 | B. | BaCl2溶液 | C. | NaOH溶液 | D. | Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
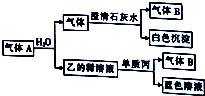 将一黑色固体单质甲投入乙的浓溶液中共热,剧烈反应产生混合气体A,A存在如图转化关系,试回答下列问题:
将一黑色固体单质甲投入乙的浓溶液中共热,剧烈反应产生混合气体A,A存在如图转化关系,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 电解质溶液 | 阳极 | 阴极 | 加入的物质 | |
| A | NaCl溶液 | 碳 | 铁 | 盐酸 |
| B | 稀硫酸 | 铜 | 碳 | 水 |
| C | 硫酸铜溶液 | 铜 | 碳 | 硫酸铜 |
| D | NaOH溶液 | 碳 | 铁 | 水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
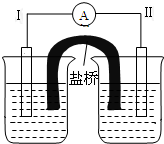 根据反应Fe+Fe2(SO4)3=3FeSO4设计的双液原电池如图所示.
根据反应Fe+Fe2(SO4)3=3FeSO4设计的双液原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,粗铜作阴极 | |
| B. | 电解精炼铜时,溶液浓度基本不变 | |
| C. | 在铁制容器上镀铜时,可用CuSO4溶液作电镀液 | |
| D. | 在铁制容器上镀铜时,铁制容器连接外接电源的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18H2O含有的氢原子数目为NA | |
| B. | 1molFe与足量盐酸反应失去的电子数为3NA | |
| C. | 标准状况下,22.4L等物质的量的CO2和O2混合气体中含有氧原子数为2NA | |
| D. | 2mol•L-1NaCl溶液中含有Na+个数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com