
| A. | 熔融不导电 | B. | 水溶液不导电 | ||
| C. | 熔点比BeBr2高 | D. | 不与NaOH溶液反应 |
分析 AlCl3的结构和化学性质:氯化铝是共价化合物,熔融态不导电,铝离子能发生水解使溶液呈碱性,能与NaOH溶液反应生成氢氧化铝沉淀.BeCl2化学性质与AlCl3相似,以此解答该题.
解答 解:AlCl3的结构和化学性质:氯化铝是共价化合物,熔融态不导电,铝离子能发生水解使溶液呈碱性,能与NaOH溶液反应生成氢氧化铝沉淀.BeCl2化学性质与AlCl3相似,则
A.BeCl2为共价化合物,故熔融态不导电,故A正确;
B.在水溶液中可电离,溶液导电,故B错误;
C.BeCl2和BeBr2为分子晶体,BeBr2相对分子质量大于BeCl2,故BeCl2熔点比BeBr2低,故C错误;
D.能与NaOH溶液反应生成氢氧化铍沉淀,故D错误,
故选A.
点评 本题考查元素周期表的综合应用,为高频考点,侧重于学生的分析能力的考查,注意把握题给信息,掌握氯化铝的性质是解题的关键,要注意氯化铝是共价化合物.


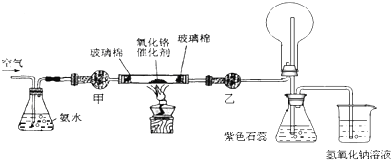
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 该反应为取代反应 | |
| B. | 维生素C易溶于水,易被氧化 | |
| C. | 1 mol有机物甲最多能和2 mol H2反应 | |
| D. | 两种有机物中含有官能团的种类相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中的原子位于同一平面 | B. | 苯的结构简式可表示为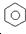 | ||
| C. | 苯中碳碳键键角为60° | D. | 苯燃烧时能产生大量黑烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol CH3CH2OH与Na完全反应只生成0.5 mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同 | |
| B. | 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构 | |
| C. | 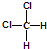 和 和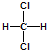 属于同一种物质,不能用来解释甲烷是一种正四面体结构 属于同一种物质,不能用来解释甲烷是一种正四面体结构 | |
| D. | 乙烯容易与溴的四氯化碳溶液发生反应,且1mol乙烯完全加成消耗1mol溴单质,证明乙烯分子里含有一个碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取乙酸乙酯时,先将1体积的酒精倒入3体积的浓硫酸中 | |
| B. | 配制银氨溶液时,将稀氨水滴加到硝酸银溶液中至白色沉淀恰好溶解为止 | |
| C. | 实验室做钠与乙醇的实验时,余下的钠投入废液缸中 | |
| D. | 制乙烯时,用量程为100℃的温度计代替量程为300℃的温度计,测反应液的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①④⑤ | C. | ②③⑤ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键只存在于分子内,分子间作用力只存在于分子间 | |
| B. | 冰变为液态水时,共价键没有被破坏 | |
| C. | 液态氟化氢中存在氢键,所以其分子比氯化氢稳定 | |
| D. | 物质在溶于水的过程中,化学键一定会被破坏或改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com