
【题目】某无色溶液中只可能溶有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子中的几种离子。为分析其组成,现进行如下实验:
等离子中的几种离子。为分析其组成,现进行如下实验:
![]() 取10mL该溶液于试管中滴加足量的
取10mL该溶液于试管中滴加足量的![]() 溶液,加稀硝酸酸化后过滤得到
溶液,加稀硝酸酸化后过滤得到![]() 白色沉淀甲.
白色沉淀甲.
![]() 取上述反应后的滤液,加入
取上述反应后的滤液,加入![]() 溶液未见沉淀产生.
溶液未见沉淀产生.
![]() 另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加入NaOH的物质的量为
另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加入NaOH的物质的量为![]() 时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为
时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为![]() 假设丙全部逸出
假设丙全部逸出![]() ,最后沉淀完全溶解。
,最后沉淀完全溶解。
下列推断正确的是![]()
A.肯定有![]() 、
、![]() 、
、![]() 、
、![]()
B.肯定有![]() 、
、![]() 、
、![]()
C.肯定没有![]() 、
、![]() 、
、![]()
D.肯定没有![]() 、
、![]() 、
、![]()
【答案】B
【解析】
溶液无色,说明不含![]() ;
;
![]() 取10mL该溶液于试管中滴加
取10mL该溶液于试管中滴加![]() 溶液,加稀硝酸酸化后过滤得到
溶液,加稀硝酸酸化后过滤得到![]() 白色沉淀甲,说明甲为
白色沉淀甲,说明甲为![]() ,原溶液中含有
,原溶液中含有![]() ;
;
![]() 向滤液中加入
向滤液中加入![]() 溶液未见沉淀产生,说明不含有
溶液未见沉淀产生,说明不含有![]() 、
、![]() ;
;
![]() 另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解,说明含有
另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解,说明含有![]() 、
、![]() ,不含
,不含![]() ,因为能与碱共热生成气体的只有
,因为能与碱共热生成气体的只有![]() ,氢氧化镁不溶于氢氧化钠溶液,
,氢氧化镁不溶于氢氧化钠溶液,![]() 能与氢氧化钠溶液反应生成沉淀又能完全溶解,铝离子与碳酸氢根离子能发生双水解反应而不能大量共存,故不含
能与氢氧化钠溶液反应生成沉淀又能完全溶解,铝离子与碳酸氢根离子能发生双水解反应而不能大量共存,故不含![]() ;根据氢氧化铝沉淀
;根据氢氧化铝沉淀![]() 和标况下氨气为
和标况下氨气为![]() ,利用元素守恒可知有
,利用元素守恒可知有![]() ,
,![]()
![]() ,再根据电荷守恒可推知含有
,再根据电荷守恒可推知含有![]() ;
;
综上分析可知一定含有的离子为![]() 、
、![]() 、
、![]() 、
、![]() ,一定不含有的离子为
,一定不含有的离子为![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。
。
答案选B。


科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种均可溶于水的固体物质,是由以下提供的几种离子组成![]() 每种离子只能用一次
每种离子只能用一次![]() :
:
阳离子 |
|
阴离子 |
|
现分别进行如下实验:
![]() 将D与E的溶液混合加热,产生有刺激性气味的气体
将D与E的溶液混合加热,产生有刺激性气味的气体
![]() 将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
![]() 在常温下用pH试纸测定溶液A的
在常温下用pH试纸测定溶液A的![]()
下列说法不正确的是![]()
A.物质E的化学式为![]() B.物质D中一定含有
B.物质D中一定含有![]()
C.难以确定物质A的组成D.物质C的化学式是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合如图的反应是( )

A.X(g)+3Y(g)![]() 2Z(g) ΔH>0
2Z(g) ΔH>0
B.X(g)+3Y(g)![]() 2Z(g) ΔH<0
2Z(g) ΔH<0
C.X(g)+2Y(g)![]() 3Z(g) ΔH<0
3Z(g) ΔH<0
D.X(g)+2Y(g)![]() 3Z(g) ΔH>0
3Z(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列溶液的有关计算。
(1)某H2SO4溶液的浓度是0.005molL-1;
①此溶液的pH=___;
②该溶液中由水电离的c(H+)为___。
③用水稀释到原来体积的100倍,pH=___。
(2)0.001mol/L的NaOH溶液, pH=___;
(3)0.015mol/L的H2SO4与0.01mol/L的NaOH等体积混合,混合液pH=___。
(4)把pH=3的H2SO4溶液和pH=10的NaOH溶液混合,两者恰好中和,则两种溶液的体积比应是___。
A.10∶1 B.1∶10 C.1∶100 D.1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组拟探究CO2和锌粒反应是否生成CO,已知CO能与银氨溶液反应产生黑色固体。实验装置如图所示,下列说法正确的是 ( )

A.实验开始时,先点燃酒精灯,后打开活塞K
B.b、c、f中试剂依次为氢氧化钠溶液、浓硫酸、银氨溶液
C.a中所发生反应的离子方程式是CaCO3+2H+=CO2↑+Ca2++H2O
D.装置e的作用是收集一氧化碳气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
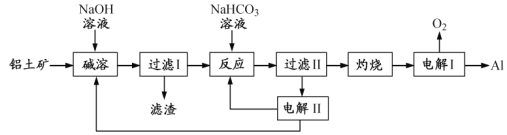
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
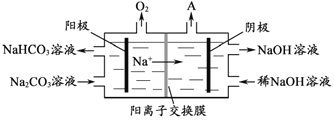
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为_____________________,阴极产生的物质A的化学式为____________。
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室用环己醇合成环己烯的反应实验装置如图所示:

可能用到的有关数据如下:

(1)仪器a的名称为_____,向仪器a中加入①环己醇②浓硫酸③碎瓷片的合理顺序为_____(填序号),碎瓷片的作用是_____。
(2)装置b中冷凝水应从_____口进入;该反应温度计的数值控制不超过90℃,温度计水银球放在支管口处的目的是____。
(3)由环己醇制取环己烯的方程式_____,实验中最容易产生的副产物的结构简式为____。
(4)分离提纯时,将生成粗产品倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后再加入无水氯化钙颗粒。分液漏斗在使用前须清洗干净并_____,向分液漏斗中粗产品加入5%碳酸钠溶液后的分离操作过程是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·武汉市高中毕业生五月模拟考试)草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下::
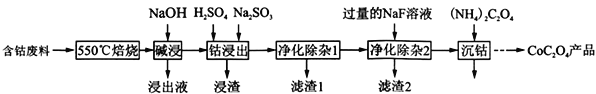
(1) “550℃焙烧”的目的是______________________;
(2)“浸出液”的主要成分是_____________________;
(3) “钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_____________________;
(4) “净化除杂1”过程中,先在40 ~ 50℃加入H2O2,其作用是___________________________(用离子方程式表示);再升温至80 ~ 85℃,加入Na2CO3溶液,调pH至4.5,“滤渣1”主要成分的是_____________________。
(5) “净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l05mol /L,则滤液中 c(Mg2+)为______________ [已知Ksp(MgF2) =7.35×1011、Ksp(CaF2) =1.05×1010]。
(6)为测定制得样品的纯度,现称取1.00 g样品,将其用适当试剂转化,得到草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0. 1000 mol/L KMnO4溶液滴定,达到滴定终点时,共用去KMnO4溶液26.00 mL,则草酸钴样品的纯度为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次递增的前四周期元素。A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层P能级比S能级多1个电子;F原子的最外层电子数与A相同,其余各层均充满。据此回答下列问题。
(1)F元素形成的高价基态离子的核外电子排布式为__________。
(2)E的一种具有强还原性的氧化物分子的VSEPR模型为__________。
(3)C、D、E元素的第一电离能由大到小的顺序是__________。(用元素符号表示)
(4)A和D形成的18电子化合物难溶于BE2,其理由是__________,此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为__________
(5)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________。
(6)F与C形成化合物的晶胞如图所示,该化合物的化学式为_____________,C离子的配位数是_____________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com