
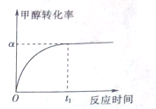
 乙酸是重要的有机化工原料,可由乙烯氧化法、甲醛羟基化法等方法生产.回答下列问题:
乙酸是重要的有机化工原料,可由乙烯氧化法、甲醛羟基化法等方法生产.回答下列问题:分析 (1)乙烯在催化剂存在条件下与氧气反应生成乙醛,乙醛与氧气进一步发生氧化反应生成乙酸,据此书写方程式;
(2)根据盖斯定律①+②+③得到CH3OH(g)+CO(g)?CH3COOH(g)进行计算;
(3)根据乙酸溶于水成酸性检验;
(4)①根据该反应为气体体积减小的放热反应分析,要想提高转化率,则使平衡向正反应方向移动;
②根据K=$\frac{c(CH{\;}_{3}COOH)}{c(CH{\;}_{3}OH)c(CO)}$进行计算.
解答 解:(1)乙烯在催化剂存在条件下与氧气反应生成乙醛,方程式为CH2=CH2+O2$\stackrel{催化剂}{→}$CH3CHO,乙醛与氧气进一步发生氧化反应生成乙酸,该反应为2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH,故答案为:为CH2=CH2+O2$\stackrel{催化剂}{→}$CH3CHO;2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
(2)①CH3OH(g)+HI(g)?CH3I(g)+H2O(g)△H1
②CH3I(g)+CO(g)?CH3COI(g)△H2
③CH3COI(g)+H2O(g)?CH3COOH(g)+HI(g)△H3
①+②+③得CH3OH(g)+CO(g)?CH3COOH(g)△H=△H1+△H2+△H3;根据反应碘代甲烷为反应①的产物,反应②的反应物,所以反应过程中的碘代甲烷是中间产物;
故答案为:△H1+△H2+△H3;中间产物;
(3)因为乙酸溶于水成酸性,所以用紫色石蕊试液检验即可,具体操作为取少量产品溶于水配成溶液,滴加紫色石蕊试液,如果变红,则说明含有乙酸成分;
故答案为:取少量产品溶于水配成溶液,滴加紫色石蕊试液,如果变红,则说明含有乙酸成分;
(4)①要想提高转化率,则使平衡向正反应方向移动,又该反应为气体体积减小的放热反应,所以可以增加压强或者降低温度,故答案为:增加压强;降低温度;
②设开始时充入CH3OH(g)的浓度为1mol/L,则CO(g)的浓度为λmol/L,
由 CH3OH(g)+CO(g)?CH3COOH(g)
开始 1mol/L λmol/L 0
转化 α α α
平衡 1-α λ-α α
所以K=$\frac{c(CH{\;}_{3}COOH)}{c(CH{\;}_{3}OH)c(CO)}$=$\frac{α}{(1-α)×(λ-α)}$,
故答案为:$\frac{α}{(1-α)×(λ-α)}$.
点评 本题考查了有机反应方程式的书写、盖斯定律的应用以及化学平衡常数的计算,建立三段式是解答平衡计算是关键,题目难度中等.


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:高中化学 来源: 题型:选择题
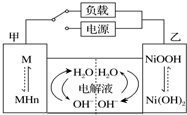 发展混合动力车是实施节能减排的重要措施之一.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗.混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,电解液为碱液(主要为KOH)(见图).镍氢电池充放电原理总反应式为:H2+2NiOOH$?_{充电}^{放电}$2Ni(OH)2.下列有关混合动力车的判断正确的是( )
发展混合动力车是实施节能减排的重要措施之一.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗.混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,电解液为碱液(主要为KOH)(见图).镍氢电池充放电原理总反应式为:H2+2NiOOH$?_{充电}^{放电}$2Ni(OH)2.下列有关混合动力车的判断正确的是( )| A. | 在刹车和下坡时,甲电极的电极反应式为:H2+2OH--2e-═2H2O | |
| B. | 在上坡或加速时,甲电极周围溶液的pH将减小 | |
| C. | 在上坡或加速时,溶液中的K+向甲电极迁移 | |
| D. | 在刹车和下坡时,乙电极增重 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
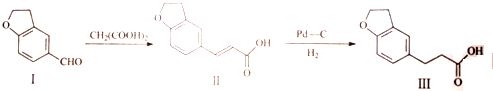
| A. | 可用浓溴水区分化合物Ⅱ和化合物Ⅲ | |
| B. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| C. | 1mol化合物Ⅰ最多能与3molH2发生加成反应 | |
| D. | 与化合物Ⅰ互为同分异构体,且分子含有2个醛基的芳香族化合物有10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y均能燃烧,都有大量浓烟产生 | |
| B. | X既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,还能发生加聚反应 | |
| C. | Y属于不饱和烃 | |
| D. | Y的二氯代物有三种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用蒸馏分离有机物时,明火尽量与接液器保持一定距离 | |
| B. | 做焰色反应实验时,铂丝需要在硫酸中蘸洗 | |
| C. | 实验室制取氨气时,收集装置必须洗净但无需干燥 | |
| D. | 甲烷与氧气反应时,需要黑纸遮挡避免灯光照射 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
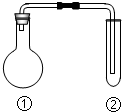 下列选项中的反应、现象与结论完全一致的是(夹持、加热装置已略去)( )
下列选项中的反应、现象与结论完全一致的是(夹持、加热装置已略去)( )| ①中的反应 | ②中的现象 | 结论 | |
| A | MnO2与浓盐酸加热 | KI淀粉溶液很快变蓝 | Cl2有氧化性 |
| B | Cu与浓硫酸加热 | 溴水褪色 | SO2有漂白性 |
| C | Na2CO3与醋酸溶液 | 苯酚钠溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 电石与饱和食盐水 | 酸性高锰酸钾溶液褪色 | 乙炔有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 气态氢化物的稳定性:Z<M | |
| C. | 简单离子半径由大到小的顺序是:Z>M>Y | |
| D. | 等浓度的X2Z与Y2Z的溶液中,水的电离程度:X2Z<Y2Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | R | |
| 主要化合价 | -4,+4 | -4,+4 | -2,+6 | -1,+7 |
| A. | 非金属性:Z<R<Y | |
| B. | T与R可以形成化合物:TR2 | |
| C. | X与R的单质均能使品红溶液褪色,且褪色原理相同 | |
| D. | T的最高价氧化物的水化物分别能与X、Y、Z的最高价氧化物反应 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第13次周测理科综合化学试卷 题型:实验题
冰晶石(Na3 AlF6)难溶于水,广泛应用于铝的冶炼。工业上用萤石(CaF2)为原料生产Na3 AIF6:
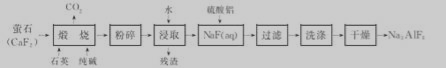
回答下列问题:
(1)Na3AIF6为助溶剂,冶炼铝的化学方程式为 。
(2)写出煅烧时总反应的化学方程式为________。
(3)煅烧后的固体在浸取前进行粉碎的目的是____,为达到相同目的,常温浸取时还可采取的措施是____。
(4)写出向NaF溶液中加入硫酸铝溶液发生反应的离子方程式:____。NaF溶液呈碱性,用离子方程式表示其原因: ,因此在按化学计量加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,否则可能产生副产物 。
(5)97.5kg含CaF280%萤石(杂质不含氟元素)理论上可生产Na3 AIF6 kg(设生产过程中的每一步含氟物质均完全转化)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com