

| 1 |
| 2 |
| 1 |
| 2 |
| 10-14 |
| 10-pH |
| 1 |
| 2 |
| 1 |
| 2 |
| 10-14 |
| 10-pH |
| 1 |
| 2 |
| 10-14 |
| 10-13 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ӻ����� | B������� |
| C������ | D������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��OH-+H+=H2O |
| B��H++NH3?H2O=NH4++H2O |
| C��HCl+OH-=Cl-+H2O |
| D��HCl+NH3?H2O=Cl-+NH4++H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ij�л���A�ķ����У���ṹ��ʽ��ͼ��
��ij�л���A�ķ����У���ṹ��ʽ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ȡ������Ʒ���Թ��У��� |
����ɫ���������˵����Ʒ�к���Na2CO3�� |
| �� | �а�ɫ������������Na2SO4 | |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ࡢ֬���������ʡ�ά���ء������ʣ����Σ���ˮ�ϳ�����Ӫ���أ�ʳ�����ʱ��ʹ��һЩ��ζ�����Ż��ҽ���������ͼ��
���ࡢ֬���������ʡ�ά���ء������ʣ����Σ���ˮ�ϳ�����Ӫ���أ�ʳ�����ʱ��ʹ��һЩ��ζ�����Ż��ҽ���������ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
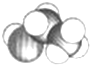 �Ҵ��������г�����һ���л�����ķ��ӽṹģ����ͼ��ʾ��
�Ҵ��������г�����һ���л�����ķ��ӽṹģ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ��������Һ�ķ�Ӧ��H++OH-�TH2O | ||||
| B��ͭ���Ȼ�����Һ��Ӧ��Fe3++Cu�TFe2++Cu2+ | ||||
C������������Ũ����ķ�Ӧ��MnO2+4H++4Cl-
| ||||
| D��̼������������������Һ�ķ�Ӧ��HCO3-+OH�TCO32-+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com