
【题目】如图为几种有机化合物的结构简式:
①CH3CH=CHCH2CH3②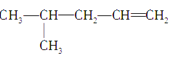 ③CH3CH2CH2CH2OH④CH3—C≡C—CH3⑤ CH3—CH2—C≡CH⑥
③CH3CH2CH2CH2OH④CH3—C≡C—CH3⑤ CH3—CH2—C≡CH⑥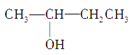 ⑦CH3CH2CH2OCH3⑧
⑦CH3CH2CH2OCH3⑧![]() ⑨CH2=CH—CH=CH2⑩ CH2=CHCH2CH2CH3
⑨CH2=CH—CH=CH2⑩ CH2=CHCH2CH2CH3
(1)属于同分异构体的是______、______、__________、__________。
(2)属于官能团位置不同的同分异构体是:________、__________、________。
(3)属于官能团类型不同的同分异构体是:____、____、____、____、____。
【答案】①⑩ ②⑧ ③⑥⑦ ④⑤⑨ ①⑩ ③⑥ ④⑤ ③⑦ ④⑨ ⑤⑨ ⑥⑦ ②⑧
【解析】
同分异构体是分子式相同,结构不同的物质互为同分异构体,碳链异构:由于分子中碳链形状不同而产生的异构现象;位置异构:由于取代基或官能团在碳链上或碳环上的位置不同而产生的异构现象,官能团异构:分子中由于官能团不同而产生的异构现象。
①CH3CH═CH﹣CH2CH3 、⑩CH2=CH﹣CH2CH2CH3分子式相同,碳碳双键位置不同,二者属于位置异构;
④CH3﹣C≡C﹣CH3,⑤CH3﹣CH2﹣C≡CH,⑨CH2=CH﹣CH=CH2,三种分子式相同、结构不同,属于同分异构体,其中④⑤碳碳三键位置不同,属于位置异构,④、⑤与⑨的官能团不同,属于官能团异构;
③CH3CH2﹣CH2﹣CH2OH、⑥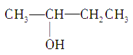 、⑦CH3CH2CH2OCH3,分子相同,结构不同,三种互为同分异构体,③⑥羟基位置不同,属于位置异构,③、⑥与⑦的官能团不同,属于官能团异构;
、⑦CH3CH2CH2OCH3,分子相同,结构不同,三种互为同分异构体,③⑥羟基位置不同,属于位置异构,③、⑥与⑦的官能团不同,属于官能团异构;
②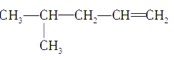 、⑧
、⑧![]() 的分子式相同,前者含有碳碳双键,或者含有环状,属于官能团异构;
的分子式相同,前者含有碳碳双键,或者含有环状,属于官能团异构;
(1)根据分析可知,互为同分异构体的有:①⑩、②⑧、③⑥⑦、④⑤⑨;
(2)属于官能团位置不同的同分异构体是:①⑩、③⑥、④⑤;
(3)属于官能团类型不同的同分异构体是:③⑦、④⑨、⑤⑨、⑥⑦、②⑧。


科目:高中化学 来源: 题型:
【题目】如图是某化工厂对海水资源综合利用的示意图。根据以上信息,判断下列相关分析不正确的是
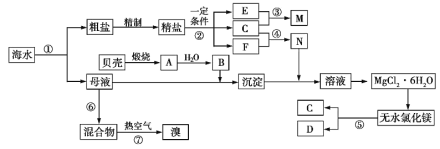
A. 上述提取Mg的流程中,没有涉及的反应类型是置换反应
B. 因氮气的化学性质相对稳定,冷却电解无水氯化镁所得的镁蒸气时,可选择氮气
C. 反应⑥所用的气态氧化剂可从本厂生产烧碱处循环利用或从本厂生产镁单质处循环利用
D. 从母液中提取Mg和Br2的先后顺序:先提取Br2,后提取Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是
A.过量的铁在1molCl2中然烧,最终转移电子数为2NA
B.在50g质量分数为46%的乙醇水溶液中,含氢原子总数为6NA
C.5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
D.1L1mol/LNaCl溶液和1L1mol/LNaF溶液中离子总数:前者小于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Kap[Mg(OH)2]=1.8×10-11,Kap[Al(OH)3]=3.0×10-34,Kap[Fe(OH)3]=4.0×10-38。)
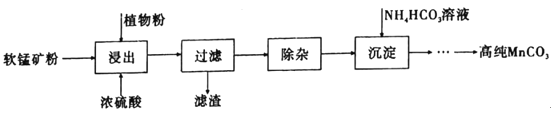
A.浸出时加入植物粉的作用是作为还原剂
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.试剂X可以是MnO、MnO2、MnCO3等物质
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。

已知:CoC2O4·2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O42-离子生成Co(C2O4)n2(n-1)-而溶解。
(1)“还原酸浸”过程中,LiCoO2发生反应的离子方程式为:___,该过程温度通常控制在40℃以下的原因是:___。
(2)“除铝铁”过程的两种试剂的作用分别是___,___。
(3)“除铜”所用试剂X为H2S,试写出该反应的离子方程式:___。并计算室温下该反应的平衡常数K=___,已知:25℃时Kap(CuS)=8.5×10-45,已知H2S在水中的的电离常数:K1=1.3×10-7,K2=7.l×10-15
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:

①随n(C2O42-):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因___。
②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是___。
(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10-1mol·L-1,部分锂盐的溶解度数据如下表所示。

结合数据分析,沉锂过程所用的试剂b是___(写化学式),相应的操作方法:向滤液a中加入略过量的试剂b,搅拌,___,___,洗涤干燥。检验沉淀洗净的方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列有机物的结构简式,若有违反系统命名者请予以纠正。
(1)3,5-二甲基己烷________________,正确名称:________________
(2)3,3,4,4-四甲基-2-乙基戊烷________________,正确名称:________________
(3)4,4,5,5-四甲基-3-丙基己烷________________,正确名称:________________
(4)2,3,4,5-四甲基-3-乙基-5-丙基庚烷____________,正确名称:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一套实验室制取乙烯并验证乙烯具有还原性的实验装置。请回答:
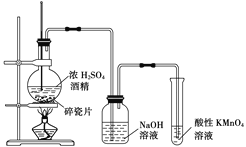
甲 乙
(1)实验步骤:
①组装仪器,检验装置的______;
②在各装置中注入相应的试剂(如图所示);
③加热,使温度迅速升到______℃;实验时烧瓶中液体混合物逐渐变黑。
(2)能够说明乙烯具有还原性的现象是:___________________________________;装置甲的作用是:____________________。若无甲装置,是否也能检验乙烯具有还原性?____,理由是:_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。
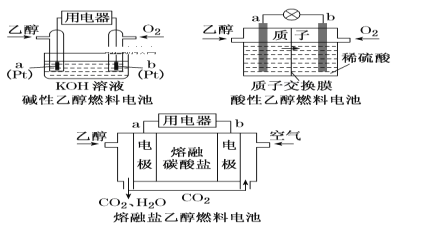
①三种乙醇燃料电池中正极反应物均为______________________;
②碱性乙醇燃料电池中,电极a上发生的电极反应式为_______________________________;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上发生的电极反应式为________。
(2)天然气既是高效洁净的能源,也是重要的化工原料。
①甲烷与氯气光照条件下的产物有多种,其中三氯甲烷(氯仿)可用作麻醉剂。氯仿分子的空间构型为_______________。
②甲烷高温分解生成氢气和炭黑。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com