
下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶 质 HCl NaOH CH3COOH HNO3
溶质的质量分数/% 36.5 40 60 63
物质的量浓度/mol•L﹣1 11.8 14.3 10.6 13.8
这4种溶液中密度最小的是()
A. HCl B. NaOH C. CH3COOH D. HNO3
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:
近年来,由CO2催化加氢合成甲醇的相关研究受到越来越多的关注.该方法既可解决CO2废气的利用问题,又可开发生产甲醇的新途径,具有良好的应用前景.已知4.4g CO2气体与H2经催化加成生成CH3OH气体和水蒸气时放出4.95kJ的能量.
(1)该反应的热化学方程式为:
(2)在270℃、8MPa和适当催化剂的条件下,CO2的转化率达到22%,则4.48m3(已折合为标准状况)的CO2能合成CH3OH气体的物质的量是 ,此过程中能 放出热量 kJ.
(3)又已知H2O(g)═H2O(l)△H=﹣44kJ/mol,则22g CO2气体与H2反应生成CH3OH气体和液态水时放出热量为 .
(4)根据该反应特点,有利于甲醇合成的条件是 .
A.高压高温 B.低压高温
C.高压低温 D.低压低温.
查看答案和解析>>
科目:高中化学 来源: 题型:
类推的思想方式在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证。以下类推的结论中正确的是( )
A.SO2能使酸性KMnO4溶液褪色,故CO2也能使酸性KMnO4溶液褪色
B.盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气
C.SO2能使品红溶液褪色,故CO2也能使品红溶液褪色
D.常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
在银锌原电池中,以硫酸铜为电解质溶液,锌为极,电极上发生的是反应(“氧化”或“还原”),电极反应式为,锌片上观察到的现象为.银为正极,电极上发生的是反应(“氧化”或“还原”),电极反应式是,银片上观察到的现象是.
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置进行相应实验,能达到实验目的是(夹持装置未画出)()
A. 
用装置甲检验溶液中是否有K+
B. 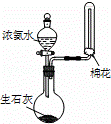
用装置乙制取并收集少量NH3
C. 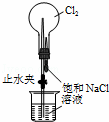
用装置丙进行喷泉实验
D. 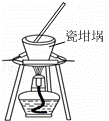
用装置丁加热熔融NaOH固体
查看答案和解析>>
科目:高中化学 来源: 题型:
FeS 与一定浓度的HNO3 反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO 和H2O,当NO2、N2O4、NO 的物质的量之比为1:1:1 时,实际参加反应的FeS 与HNO3的物质的量之比为()
A. 1:6 B. 1:7 C. 2:11 D. 16:25
查看答案和解析>>
科目:高中化学 来源: 题型:
硝铝[Al(NO3)3]是一种常用媒染剂.工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3•9H2O]的流程如图甲:
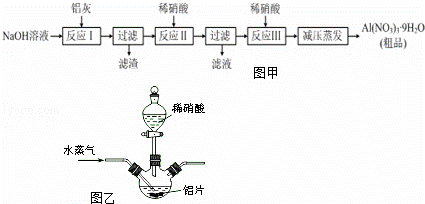
(1)写出反应Ⅰ的离子方程式: )(任写一个).
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是),可采取的措施为
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的是.
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是.
(5)若用图乙所示实验装置制取Al(NO3)3,通入水蒸气的作用是.
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A+3B═2C+2D在四种不同的情况下的反应速率如下,最快的是()
A. v(A)=0.15mol/(L•min) B. v(B)=0.6mol/(L•min)
C. v(c)=0.4mol/(L•min) D. v(D)=0.45mol/(L•min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com