
| A.①④⑤ | B.①⑤ | C.②③④ | D.④⑤ |
科目:高中化学 来源:不详 题型:实验题
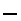 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O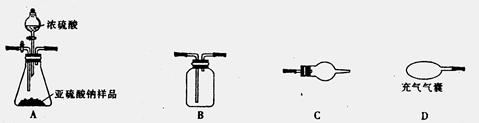
| 实验装置(填字母) | D | | | C | | | |
| 装置中所盛药品(填序号) | ④ | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
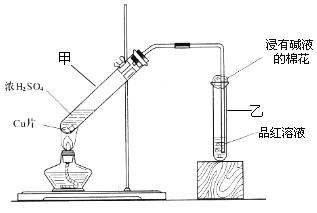
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
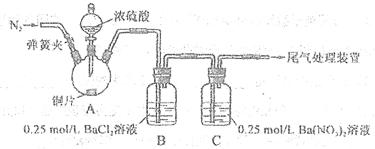
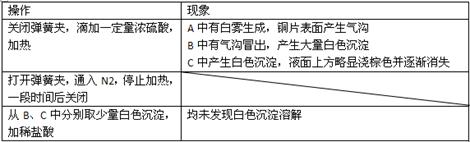
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
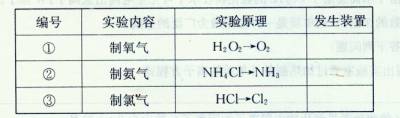
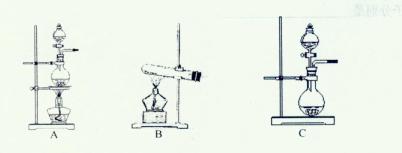
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
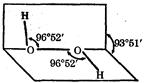
 ,并在方程式上标出电子转移的方向与数目。
,并在方程式上标出电子转移的方向与数目。| A.MnO2 | B.H2S | C.稀H2SO4 | D.NaHCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com