
| A、1:10 | B、1:5 |
| C、1:2 | D、2:1 |


科目:高中化学 来源: 题型:
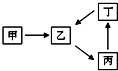 甲、乙、丙、丁四种物质转化关系如图.已知甲是地壳中含量最高的元素组成的单质.
甲、乙、丙、丁四种物质转化关系如图.已知甲是地壳中含量最高的元素组成的单质.| 温度/℃ | 400 | 450 | 500 | 550 | 600 | 650 |
| 转化率/% | 99.2 | 97.5 | 93.5 | 85.6 | 73.7 | 58.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 |
| B、甲酸与乙二酸互为同系物 |
| C、用浓Na2SO4、CuSO4溶液或浓硝酸溶液使蛋清液发生盐析,进而分离、提纯蛋白质 |
D、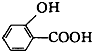 (水杨酸)与足量的NaHCO3溶液反应可生成 (水杨酸)与足量的NaHCO3溶液反应可生成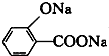 、CO2和H2O 、CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
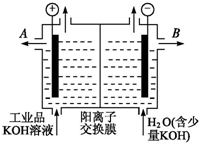 铝和氢氧化钾都是重要的工业产品.请回答:
铝和氢氧化钾都是重要的工业产品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
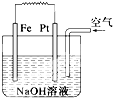
| A、这是电解NaOH溶液的装置 |
| B、该装置中Pt为正极,电极反应为O2+2H2O+4e-═4OH- |
| C、该装置中Fe为负极,电极反应为Fe-2e-═Fe2+ |
| D、这是一个原电池装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | C | |
| B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com