
��18 gͭ�����Ļ����Ͷ��200 mLϡ������,��ַ�Ӧ��õ���״����2.24 L NO,ʣ��9.6 g����;��������200 mL��Ũ�ȵ�ϡ����,������ȫ�ܽ�,�ֵõ���״����2.24 L NO������Ӧ�����Һ�м���KSCN��Һ,��Һ�����,������˵������ȷ����(����)
| A��ԭ�������ͭ������0.15 mol | B��ϡ��������ʵ���Ũ��Ϊ1 mol��L-1 |
| C����һ��ʣ��9.6 g����Ϊͭ���� | D���ټ�������200 mLϡ����,����õ���״����2.24 L NO |
A
���������������Ӧ�����Һ�м���KSCN��Һ,��Һ����죬˵������Һ�д��ڵ�������Fe2+����Һ�д���Fe2+��Cu2+�����μ��������ͬ��������NO�����ʵ�����ͬ����ת�Ƶĵ��ӵ����ʵ���Ҳ��ͬ��ÿһ�η�Ӧ����NO�����ʵ���Ϊ2.24L��22.4L/mol=0.1mol,����ת��Ϊ0.1mol��3=0.3mol.���ڽ������Fe>Cu,���������ܽ���ǽ���Fe,���ݷ�Ӧ����ʽ��3Fe��8HNO3(ϡ)=3Fe(NO3)2��2NO����4H2O����֪���ĵĽ���Fed�����ʵ���Ϊ3/2��0.1mol=0.15 mol.��ʣ��Ľ�������Cu����n(Cu)=" 9.6" g��64g/mol="0.15" mol;����Cu��+2�۽��������Ե���ת����ĿΪ0.15 mol��2=0.3mol������������Ǻϡ����ԭ�������ͭ������0.15 mol��ÿһ�μ�����������ʵ���Ϊ8/2��0.1mol=0.4mol.�����������ʵ���Ũ��Ϊ0.4mol��0.2L=2mol/L.���ټ�������200 mLϡ���ᣬ�ᷢ����Ӧ��NO3-+4H++3Fe2+= 3Fe3++NO��+2H2O��n(Fe2+)=0.15 mol;��Ӧ��Ҫ����H+�����ʵ���Ϊ0.15 mol ��4/3=0.2mol;ʵ�ʼ����n(H+)=0.4mol��������Ҫ������˷ų������尴��Fe2+�����㡣�������ӷ���ʽ��֪�ɻ������NO�ĵ����ʵ���Ϊ0.05 mol���ڱ�״�������Ϊ1.12L�������ȷѡ��ΪA��
���㣺����ͭ�����Ļ���������ᷢ����Ӧ�������֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������������ȷ����( )
��NH3��Һ����Һ�������������
���������Ӧʱ��ϡHNO3���ܱ���ԭΪ���ͼ�̬����ϡHNO3������ǿ��ŨHNO3
����������ֽ⣬��������̬����ʱҪ�ܷⱣ�棬����������ͨ�紦
��ϡHNO3�ͻ��ý�����Ӧʱ��Ҫ�õ�����
| A���٢� | B���ڢ� | C���٢ڢۢ� | D��������ȷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���г�������ȷ�����������ϵ����
| ѡ�� | ������ | ������ |
| A | H2O2��SO2����ʹ���Ը��������ɫ | ǰ�߱��ֳ���ԭ�Ժ��߱��ֳ�Ư���� |
| B | �����������ڿ����н����䰵 | �����˻�ѧ��ʴ |
| C | SiO2��������ἰ�Ӧ | SiO2������������ |
| D | BaSO4������Һ�м��뱥��Na2CO3��Һ�а�ɫ���� | ˵��Ksp(BaSO4)����Ksp(BaCO3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�йذ���˵������ȷ����
| A��NH3��4��10���ӵķ��ӣ������Σ����л�ԭ�� |
| B��NH3��������ˮ��������Ȫʵ�飻������Һ����Һ������������� |
| C�������Ƿǵ���ʣ���ˮ�ǵ���� |
| D��պ��Ũ����IJ������������ɲ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
±�ؼ��γɵĻ������硰IF5��BrCl��IBr���ȳ�Ϊ±�ػ������ѧ������±�ص������ƣ������й���±�ػ���������ʵ���������������ط�Ӧ����ȷ����
| A��IF5 + 3H2O = HIO3 +5HF |
| B��3IBr +2Fe = FeI3 + FeBr3 |
| C��BrCl��������ǿ��I2 |
| D��IBr������NaOH��Һ��Ӧ����2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����й�˵������ȷ����
| A��ʵ������ȡ������Ϊ�˼ӿ췴Ӧ���ʣ�����ϡH2SO4�еμ�����Cu(NO3)2��Һ |
| B��Ϊ������¯ˮ���е�CaSO4�������ñ���Na2CO3��Һ���ݣ��ټ��������ܽ� |
C����֪NaOH(aq)��HCl(aq)��NaCl(aq)��H2O(l) ��H��-57.3 kJ��mol��1����ˮ������Ȼ�ѧ����ʽΪ��H2O(l) H+(aq)+OH-(aq)��H�� +57.3 kJ��mol��1 H+(aq)+OH-(aq)��H�� +57.3 kJ��mol��1 |
| D����������������ʴ�����ⸯʴ�ĸ�����Ӧ��Ϊ��Fe-2e- ��Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���й�ϵͼ�У�A��һ�����Σ�BΪ��̬�⻯�C�ǵ��ʣ�F��ǿ�ᡣ��X������ǿ�ỹ��ǿ��ʱ��������ͼ��ʾ��ת����ϵ��������Ӧ�������������������ȥ����������˵���в���ȷ����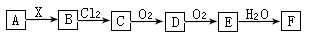
| A����X��ǿ��ʱ��A��F����ͬһ��Ԫ�أ�F����ΪH2SO4 |
| B����X��ǿ��ʱ��A��F����ͬһ��Ԫ�أ�F����ΪHNO3 |
| C��B��Cl2�ķ�ӦΪ������ԭ��Ӧ |
| D����X��ǿ��ʱ��������CΪ��̬���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ڸ�ѹ�µ�����ۺ����ɸ߾۵������ָ߾۵��ľ�����ÿ����ԭ�Ӷ�ͨ������������������ԭ�ӽ�ϲ���ռ䷢չ����������״�ṹ����ͼ������֪������N �� N���ļ���Ϊ160kJ��mol��1 ����N �� N�ļ���Ϊ942kJ��mol��1 ���������й�˵����ȷ���� �� )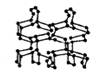
| A���߾۵��뵪����Ϊͬλ�� |
| B��14g�߾۵���3.01��1023����ԭ�� |
| C���߾۵��е�ԭ�Ӽ�Ļ�ѧ��Ϊ�Ǽ��Լ� |
| D���߾۵�ת��ɵ�����������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���³�ѹ�£������ݻ���ͬ����ƿ�зֱ�ʢ��X��Y�������壬����a��ʹ����ƿ�ڵ�������ͨ����������ڵ�ѹǿ�ɴ�С��˳��������ȷ����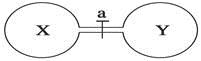
| ��� | �� | �� | �� | �� |
| ����X | HI | NH3 | H2 | NO |
| ����Y | Cl2 | HCl | Cl2 | O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com