
(1)在所给5种物质与水反应的产物中,属于最高价氧化物对应水化物的是________,属于无氧酸的是________。
(2)分别将0.01 mol这5种物质放入0.1 L水中反应,结果使溶液的pH接近3的是________。
(1)H4SiO4 HBr和HCl
(2)CH3COOOCCH3
解析:根据水解反应规律,写出有关反应的化学方程式为:IBr+H2O====HIO+HBr,SiCl4+4H2O====H2SiO4↓+4HCl,PCl3+3H2O====H3PO3+3HCl,CH3COCl+H2O![]() CH3COOH+HCl,
CH3COOH+HCl,
CH3COOOCCH3+H2O![]() 2CH3COOH。
2CH3COOH。
上述反应产物中属于最高价氧化物对应水化物的是H4SiO4,属于无氧酸的是HBr和HCl。5个反应中前4个反应都生成了强酸,只有第五个反应中的CH3COOH是弱酸。0.01 mol CH3COOOCCH3与水反应生成0.2 mol CH3COOH,形成的溶液约为0.1 L,CH3COOH溶液浓度约为0.2 mol·L-1。弱电解质难电离,大约有1%的CH3COOH发生电离,溶液中的H+浓度约为0.002 mol·L-1,pH接近3。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
①IBr+H2O====HIO+HBr
②![]() +2H+====S+SO2↑+H2O
+2H+====S+SO2↑+H2O
③![]() +4H2O2+2H+====2CrO5+5H2O
+4H2O2+2H+====2CrO5+5H2O
④2HFO====2HF+O2↑
A.①②③④ B.②③④ C.④ D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
已知IBr、SiCl4、PCl3、CH3COCl、CH3COOOCCH3常温下很容易与水反应,反应方式与盐类水解类似。
(1)在所给5种物质与水反应的产物中,属于最高价氧化物对应水化物的是________,属于无氧酸的是________。
(2)分别将0.01mol这5种物质放入0.1L水中反应,结果使溶液的pH接近3的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用“三氯氢硅还原法”制备纯硅的工业流程如图:
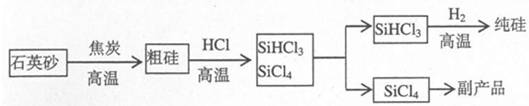
(1)石英砂的主要成分是 (填化学式),在制备粗硅时焦炭的作用是 。
(2)制备三氯氢硅的反应:
Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g)
SiHCl3(g)+H2(g) ![]()
伴随的副反应为:
Si(s)+4HCl(g) ![]() SiCl4(g)+2H2(g)
SiCl4(g)+2H2(g) ![]()
已知SiHCl3和SiCl4常温下均为液体,工业上分离SiHCl3和SiCl4的操作方法
为 ;
写出SiHCl3(g)和HCl反应生成SiCl4(g)和H2的热化学方程式 。
(3)该生产工艺中可以循环使用的物质是 。
(4)实验室用SiHCl3与过量H2反应制备纯硅的装置如下图(热源及夹持装置略去).已知SiHCl3能与H2O强烈反应,在空气中易自燃。
①装置B中的试剂是 (填名称),装置C中的烧瓶需要加热,其目的是 。
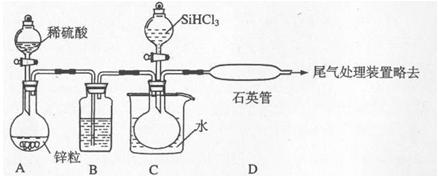
②实验中先让稀硫酸与锌粒反应一段时间后,再加热C、D装置的理由是 ,装置D中发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2011届广东省茂名市高三第一次模拟考试(理综)化学部分 题型:实验题
工业上用“三氯氢硅还原法”制备纯硅的工业流程如图: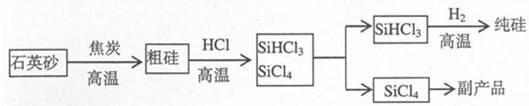
(1)石英砂的主要成分是 (填化学式),在制备粗硅时焦炭的作用是 。
(2)制备三氯氢硅的反应:
Si(s)+3HCl(g) SiHCl3(g)+H2(g)
SiHCl3(g)+H2(g) 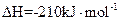
伴随的副反应为:
Si(s)+4HCl(g) 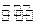 SiCl4(g)+2H2(g)
SiCl4(g)+2H2(g) 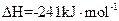
已知SiHCl3和SiCl4常温下均为液体,工业上分离SiHCl3和SiCl4的操作方法
为 ;
写出SiHCl3(g)和HCl反应生成SiCl4(g)和H2的热化学方程式 。
(3)该生产工艺中可以循环使用的物质是 。
(4)实验室用SiHCl3与过量H2反应制备纯硅的装置如下图(热源及夹持装置略去).已知SiHCl3能与H2O强烈反应,在空气中易自燃。
①装置B中的试剂是 (填名称),装置C中的烧瓶需要加热,其目的是 。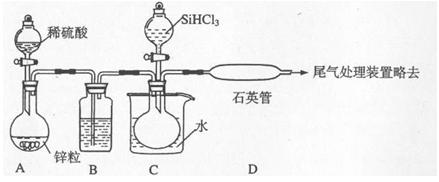
②实验中先让稀硫酸与锌粒反应一段时间后,再加热C、D装置的理由是 ,装置D中发生反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com