
为了说明影响化学反应速率快慢的因素,甲、乙、丙、丁四位同学分别设计了如下A﹣D四个实验,你认为结论不正确的是( )
|
| A. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
|
| B. | 将表面积、质量都相同的镁条和铝条分别与同浓度的盐酸反应,前者速率大于后者 |
|
| C. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
|
| D. | 相同条件下等质量的块状和粉末状大理石分别与相同浓度的盐酸反应时,粉末状的反应速率快 |
| 化学反应速率的影响因素;探究温度、压强对化学反应速率的影响. | |
| 专题: | 化学反应速率专题. |
| 分析: | A.铜不能置换出氢气; B.不同的金属,性质不同,为影响化学反应速率的主要因素; C.催化剂能加快反应速率; D.固体的表面积不同,化学反应速率不同. |
| 解答: | 解:A.铜为不活泼金属,与稀硫酸不反应,故A错误; B.镁条和铝条的活泼性不同,与相同浓度盐酸反应,镁反应速率较大,故B正确; C.催化剂能加快反应速率,在氯酸钾分解的试验中,二氧化锰起到催化剂的作用,故C正确; D.固体的表面积不同,化学反应速率不同,粉末状固体的表面积比块状固体表面积大,反应速率大,故D正确. 故选A. |
| 点评: | 本题考查外界条件对化学反应速率的影响,题目难度不大,注意B项,为易错点,物质的性质是影响化学反应速率的主要因素. |


科目:高中化学 来源: 题型:
在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g.此混合气体中C和O两种原子的物质的量之比为()
A. 4:3 B. 3:4 C. 2:1 D. 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质熔化或汽化时所克服的微粒间的作用力属同种类型的是( )
A.石英和生石灰的熔化 B.晶体硅和晶体硫的熔化
C.钠和铁的熔化 D.碘和氯化铵的汽化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式正确的是( )
|
| A. | NH3•H2O═NH4﹣+OH﹣ | B. | NaHCO3═Na++H++CO32﹣ |
|
| C. | CH3COONa═CH3COO﹣+Na+ | D. | H2S⇌2H++S2﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应mA(g)+nB(g)⇌pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3mol/L,又测得平均反应速率v(C)=2v(B).达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为
( )
|
| A. | 2A(g)+6B(g)⇌3C(g)+5D(g) | B. | 3A(g)+B(g)⇌2C(g)+2D(g) |
|
| C. | 3A(g)+B(g)⇌2C(g)+D(g) | D. | A(g)+3B(g)⇌2C(g)+2D(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应mX(g)+nY(g)⇌qZ(g)△H>0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
|
| A. | 升高温度: |
|
| B. | 降低温度,混合气体的平均相对分子质量减小 |
|
| C. | 通入稀有气体,压强增大,平衡向正反应方向移动 |
|
| D. | X的正反应速率是Y的逆反应速率的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
请回答下列问题:
(1)写出上述反应的化学方程式 .
(2)该反应的正反应是 反应(填“放热”或者“吸热”),
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 浓度/(mol•L﹣1) | 0.54 | 0.68 | 0.68 |
①此时系统温度400℃,比较正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”).
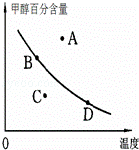
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中 点.比较图中B、D两点所对应的正反应速率B D(填“>”、“<”或“=”).理由是 .
(4)一定条件下要提高反应物的转化率,可以采用的措施是
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特利原理来解释的是( )
|
| A. | 用排饱和食盐水的方法收集氯气 |
|
| B. | 合成氨工业选择高温 |
|
| C. | 增大压强,有利于SO2和O2反应生成SO3 |
|
| D. | 在Fe3++3SCN ﹣⇌Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其Ksp=cm(An+)·cn(Bm-),称为难溶电解质的溶度积。25 ℃时,向AgCl的白色悬浊液中依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知所有的物质的颜色和溶度积如下表:
| 物质 | AgCl | AgI | Ag2S |
| 颜色 | 白 | 黄 | 黑 |
| Ksp(25 ℃) | 1.8×10-10 | 1.5×10-16 | 1.8×10-50 |
下列叙述中不正确的是( )
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.25 ℃时,饱和AgCl、AgI、Ag2S溶液中Ag+的浓度相同
D.25 ℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com