


���� ��1��һ����AlCl3��Һ�м���NaOH��Һ��������������Һ�ļ��룬��������������������������Al3++3OH-=Al��OH��3����A��ʱ�Ȼ���ǡ��ת��ΪAl��OH��3��
��2��OA�����Ȼ������������Ʒ�Ӧ�������������������Ȼ��ƣ�AB�����������������ܽ�Ĺ��̣���Ӧ����ƫ�����ƺ�ˮ��
��3��B����Һ����ΪNaAlO2��NaCl���Դ˿��ж����ӵ����ʵ���Ũ�ȣ���B�����ɵ���Һ��ͨ�������̼���ɷ�����Ӧ2AlO2-+CO2+3H2O=2Al��OH��3��+CO32-��
��4����ʼ������Ӧ��Al3++3OH-=Al��OH��3����Ȼ������Ӧ��NH4++OH-=NH3��H2O���������Ӧ��Al��OH��3+OH-�TAlO2-+2H2O�����ݷ���ʽ���������������������Һ���������ͼ��
��� �⣺��1����ͼ��֪��A�����Ȼ������������Ʒ�Ӧ���������������Ȼ��Ƶķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��AlCl3+3NaOH=Al��OH��3��+3NaCl��A��ʱ�Ѳμӷ�Ӧ��AlCl3��NaOH�����ʵ���֮��Ϊ1��3��
�ʴ�Ϊ��3��
��2��OA�����Ȼ������������Ʒ�Ӧ�������������������Ȼ��ƣ���Ӧ���ӷ���ʽΪ��Al3++3OH-=Al��OH��3����AB�����������������ܽ�Ĺ��̣���Ӧ����ƫ�����ƺ�ˮ����Ӧ�����ӷ���ʽΪ��Al��OH��3+OH-�TAlO2-+2H2O��
�ʴ�Ϊ��Al3++3OH-=Al��OH��3����Al��OH��3+OH-�TAlO2-+2H2O��
��3��B����ҺΪNaAlO2��NaCl����֪���ӵ����ʵ���Ũ������ΪNa+����B�����ɵ���Һ��ͨ�������̼���ɷ�����Ӧ2AlO2-+CO2+3H2O=2Al��OH��3��+CO32-����Ӧ���ɰ�ɫ������
�ʴ�Ϊ��Na+�����ɰ�ɫ������
��4����ʼ������Ӧ��Al3++3OH-=Al��OH��3��������0.1molAl��OH��3������0.3molNaOH������NaOH��Һ���Ϊ$\frac{0.3mol}{5mol/L}$=0.06L=60mL��Ȼ������Ӧ��NH4++OH-=NH3��H2O������0.1molNaOH������NaOH��Һ���Ϊ$\frac{0.1mol}{5mol/L}$=0.02L=20mL���������Ӧ��Al��OH��3+OH-�TAlO2-+2H2O������0.1molNaOH������NaOH��Һ���Ϊ$\frac{0.1mol}{5mol/L}$=0.02L=20mL�����ɳ��������ʵ��������NaOH��Һ����Ĺ�ϵʾ��ͼΪ��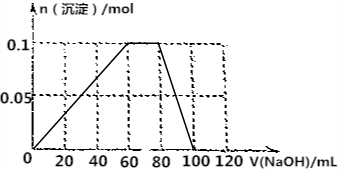 ��
��
�ʴ�Ϊ�� ��
��
���� ������ͼ��Ϊ���壬���黯ѧ����ʽ���㣬��ȷ���η����ķ�Ӧ�ǽ���ؼ���������ѧ���ķ��������ͼ��������Ŀ��飬�Ѷ��еȣ�


 Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +3NaOH$\stackrel{ˮ}{��}$
+3NaOH$\stackrel{ˮ}{��}$ +CH3COONa+2H2O
+CH3COONa+2H2O

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
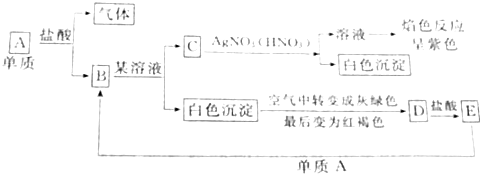 ����ͼʾ��գ�
����ͼʾ��գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��AlCl3��Һ�еμӰ�ˮ��������ɫ�������ټ������NaHSO4��Һ��������ʧ | |
| B�� | ��ʢ��Fe��NO3��2��Һ���Թ��м���0.1 mol•L-1H2SO4��Һ���Թܿڳ��ֺ���ɫ���壬˵����Һ��NO3-��Fe2+��ԭΪNO2 | |
| C�� | ��ij����ͨ��Ʒ����Һ�У�Ʒ����ɫ��˵��������һ����SO2 | |
| D�� | ��CO2ͨ��BaCl2��Һ�������ͣ�������������ͨ��SO2���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ����������֮�䲻�������㣺c��C1-����c��H+����c��NH4+����c��OH-�� | |
| B�� | ����Һ�����Ӽ����㣺c��NH4+����c��C1-����c��OH-����c��H+������Һ������һ��Ϊ��NH4Cl��NH3•H2O������ҺpH��7 | |
| C�� | ����Һ�����Ӽ����㣺c��C1-����c��NH4+����c��H+����c��OH-����Һ�����ʿ�����NH4Cl | |
| D�� | ����Һ��c��NH4+��=c��Cl-���������Һһ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com