
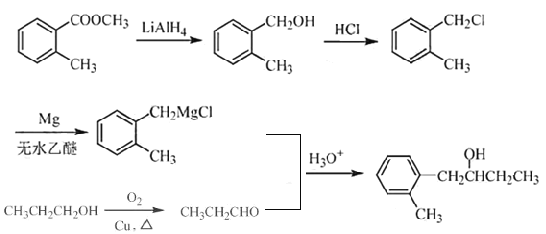
”¾ĢāÄæ”æ»ÆŗĻĪļFŹĒŗĻ³ÉŅ»ÖÖĢģȻʥą»ÆŗĻĪļµÄÖŲŅŖÖŠ¼äĢ壬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
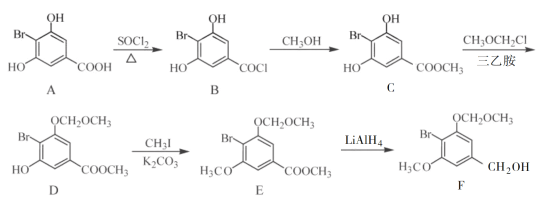
£Ø1£©EÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖ________ŗĶ________”£
£Ø2£©B”śCµÄ·“Ó¦ĄąŠĶĪŖ________”£
£Ø3£©C”śD·“Ó¦ÖŠ»įÓŠø±²śĪļX£Ø·Ö×ÓŹ½ĪŖC12H15O6Br£©Éś³É£¬XµÄ½į¹¹¼ņŹ½ĪŖ£ŗ________”£·“Ó¦D”śEµÄ·½³ĢŹ½ĪŖ______________”£
£Ø4£©CµÄŅ»ÖÖĶ¬·ÖŅģ¹¹ĢåĶ¬Ź±Āś×ćĻĀĮŠĢõ¼ž£¬Š“³öøĆĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ________”£
¢ŁÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£»
¢Ś¼īŠŌĖ®½āŗóĖį»Æ£¬ŗ¬±½»·µÄ²śĪļ·Ö×ÓÖŠ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×ÓŹżÄæ±ČĪŖ1”Ć1”£
£Ø5£©ŅŃÖŖ£ŗ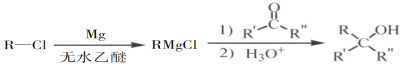 £ØR±ķŹ¾Ģž»ł£¬R'ŗĶR"±ķŹ¾Ģž»ł»ņĒā£©£¬Š“³öŅŌ
£ØR±ķŹ¾Ģž»ł£¬R'ŗĶR"±ķŹ¾Ģž»ł»ņĒā£©£¬Š“³öŅŌ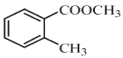 ŗĶCH3CH2CH2OHĪŖŌĮĻÖʱøµÄ
ŗĶCH3CH2CH2OHĪŖŌĮĻÖʱøµÄ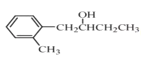 ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮŗĶÓŠ»śČܼĮČĪÓĆ£¬ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾Ąż¼ū±¾ĢāĢāøÉ£©”£____________________
ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮŗĶÓŠ»śČܼĮČĪÓĆ£¬ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾Ąż¼ū±¾ĢāĢāøÉ£©”£____________________
”¾“š°ø”æõ„»ł ĆŃ¼ü Č”“ś·“Ó¦ 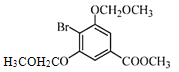
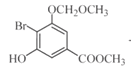 +CH3I”ś
+CH3I”ś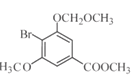 +HI
+HI 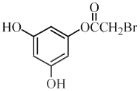
”¾½āĪö”æ
£Ø1£©øł¾ŻĢāÖŠEµÄ½į¹¹¼ņŹ½æÉĶĘÖŖEÖŠŗ¬Ńõ¹ŁÄÜĶÅ£»
£Ø2£©øł¾ŻĢāÖŠŠÅĻ¢æÉÖŖæÉĶĘÖŖB”śCµÄ·“Ó¦ĄąŠĶ£»
£Ø3£©øł¾ŻĀ·ĻßĶ¼æÉÖŖ£¬C ×Ŗ»ÆĪŖD£¬ŹĒC ÖŠŅ»øöōĒ»łÖŠµÄĒā£¬±»-CH2OCH3Č”“ś£¬¶ųC·Ö×ÓÖŠŗ¬ÓŠĮ½øöōĒ»ł£¬ĶĘ²āĮķŅ»øöōĒ»łŅ²æÉŅŌ·¢Éś“Ė·“Ó¦£¬½įŗĻø±²śĪļXµÄ·Ö×ÓŹ½ĪŖC12H15O6Br£¬æÉĶʶĻ³öXµÄ½į¹¹¼ņŹ½£»øł¾ŻĮ÷³ĢæÉÖŖ£¬·“Ó¦D”śEµÄ·“Ó¦ĪŖČ”“ś·“Ó¦£¬¾Ż“ĖŠ“³ö·“Ó¦µÄ·½³ĢŹ½£»
£Ø4£©øĆĶ¬·ÖŅģ¹¹ĢåæÉŅŌÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ŌņøĆĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ÓŠ·ÓōĒ»ł£¬ÓÖŅņĪŖĘä¼īŠŌĖ®½āŗóĖį»Æ£¬ŗ¬±½»·µÄ²śĪļ·Ö×ÓÖŠ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×ÓŹżÄæ±ČĪŖ1”Ć1£¬¾Ż“ĖæÉĶʶĻĘä½į¹¹¼ņŹ½£»
£Ø5£©øł¾ŻĀ·ĻßĶ¼ŗĶŅŃÖŖÖŠĢį¹©µÄ·“Ó¦£¬½įŗĻ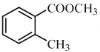 ŗĶ
ŗĶ![]() Į½ÖÖŌĮĻÉč¼ĘÖʱø
Į½ÖÖŌĮĻÉč¼ĘÖʱø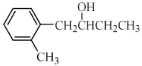 µÄĀ·Ļß”£
µÄĀ·Ļß”£
£Ø1£©øł¾ŻĢāÖŠEµÄ½į¹¹¼ņŹ½æÉÖŖ£¬EÖŠŗ¬Ńõ¹ŁÄÜĶÅĪŖõ„»ł”¢ĆŃ¼ü£»
¹Ź“š°øŹĒ£ŗõ„»ł”¢ĆŃ¼ü£»
£Ø2£©øł¾ŻĢāÖŠŠÅĻ¢æÉÖŖ£¬ÓŠ»śĪļBµÄ½į¹¹ÖŠ-COCl±äĪŖÓŠ»śĪļCÖŠµÄ-COOCH3£¬CH3O-Č”“śĮĖCl£¬ĖłŅŌB”śCµÄ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£»
¹Ź“š°øŹĒ£ŗČ”“ś·“Ó¦£»
£Ø3£©øł¾ŻĀ·ĻßĶ¼æÉÖŖ£¬C ×Ŗ»ÆĪŖD£¬ŹĒC ÖŠŅ»øöōĒ»łÖŠµÄĒā£¬±»-CH2OCH3Č”“ś£¬¶ųC·Ö×ÓÖŠŗ¬ÓŠĮ½øöōĒ»ł£¬ĶĘ²āĮķŅ»øöōĒ»łŅ²æÉŅŌ·¢Éś“Ė·“Ó¦£¬½įŗĻø±²śĪļXµÄ·Ö×ÓŹ½ĪŖC12H15O6Br£¬æÉĶʶĻ³öXµÄ½į¹¹¼ņŹ½ĪŖ £»øł¾ŻĮ÷³ĢæÉÖŖ£¬D”śEµÄ·“Ó¦ĪŖČ”“ś·“Ó¦£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗ
£»øł¾ŻĮ÷³ĢæÉÖŖ£¬D”śEµÄ·“Ó¦ĪŖČ”“ś·“Ó¦£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗ +CH3I”ś
+CH3I”ś +HI£»
+HI£»
¹Ź“š°øŹĒ£ŗ £»
£» +CH3I”ś
+CH3I”ś +HI£»
+HI£»
£Ø4£©øĆĶ¬·ÖŅģ¹¹ĢåæÉŅŌÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ŌņøĆĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ÓŠ·ÓōĒ»ł£¬ÓÖŅņĪŖĘä¼īŠŌĖ®½āŗóĖį»Æ£¬ŗ¬±½»·µÄ²śĪļ·Ö×ÓÖŠ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×ÓŹżÄæ±ČĪŖ1”Ć1£¬æÉĶʶĻĘä½į¹¹¼ņŹ½ĪŖ £»
£»
¹Ź“š°øŹĒ£ŗ £»
£»
£Ø5£©øł¾ŻĀ·ĻßĶ¼ŗĶŅŃÖŖÖŠĢį¹©µÄ·“Ó¦£¬ŅŌ ŗĶ
ŗĶ![]() ĪŖŌĮĻÖʱø
ĪŖŌĮĻÖʱø µÄĀ·ĻßĪŖ£ŗ
µÄĀ·ĻßĪŖ£ŗ £»
£»
¹Ź“š°øŹĒ£ŗ ”£
ӣ


 ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¶ŌĻą¹ŲŹµŃéµÄŠšŹö·ūŗĻŹĀŹµµÄŹĒ
A.ĢśÓėĖ®ÕōĘųŌŚøßĪĀĻĀµÄ·“Ó¦²śĪļĪŖFe3O4ŗĶH2
B.ĻņŅ»Š”ÉÕ±ÖŠ·Ö±š¼ÓČėµČĢå»żµÄĖ®ŗĶĆŗÓĶ£¬Ę¬æĢŗóŌŁĻņøĆÉÕ±ÖŠ»ŗĀżµŲ¼ÓČėŅ»ĀĢ¶¹Į£“óµÄ½šŹōÄĘ£¬æÉÄܹŪ²ģµ½µÄĻÖĻóŹĒČēĶ¼

C.ÓĆ½ą¾»µÄ²¬ĖæÕŗČ”“ż²āŅŗ£¬ÖĆÓŚ¾Ę¾«µĘ»šŃęÉĻ×ĘÉÕ£¬¹Ū²ģµ½»šŃę³Ź»ĘÉ«£¬Ōņ±ķĆ÷“ż²āŅŗÖŠŅ»¶Øŗ¬ÓŠNa+¶ų²»ŗ¬K+
D.ÓĆŪįŪöĒƼŠ×”ĀĮ²ŌŚ¾Ę¾«µĘÉĻ¼ÓČČÖĮČŪ»Æ£¬ĒįĒį»Ī¶Æ£¬ÓŠŅŗĢ¬µÄĀĮµĪĀäĻĀĄ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÖø¶Ø·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A.ĻņFeBr2ČÜŅŗÖŠĶØČėÉŁĮæCl2£ŗ2Br£+ Cl2 = Br2+ 2Cl£
B.ĻņNH4Al(SO4)2ČÜŅŗÖŠ¼ÓČė¹żĮæKOHČÜŅŗ£ŗAl3+ + 4OH- = AlO2- + 2H2O
C.ÓĆĒāŃõ»ÆÄĘČÜŅŗĪüŹÕ¹¤Ņµ·ĻĘųÖŠµÄNO2£ŗ2NO2 + 2OH- = NO3- + NO2- + H2O
D.ÓƶčŠŌµē¼«µē½āAlCl3ČÜŅŗ£ŗ2Cl- + 2H2O ![]() Cl2”ü + H2”ü + 2OH-
Cl2ӟ + H2ӟ + 2OH-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A.ŌŚ“ÖĶµÄ¾«Į¶¹ż³ĢÖŠ£¬ČōµēĀ·ÖŠ×ŖŅĘ1 mol µē×Ó£¬ŌņŃō¼«ÖŹĮæŅ»¶Ø¼õÉŁĮĖ32 g
B.·“Ó¦8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) ¦¤H<0£¬ŌņøĆ·“Ó¦Ņ»¶ØÄÜ×Ō·¢½ųŠŠ
C.1.2gµÄ½šøÕŹÆŗĶ12g µÄSiO2·Ö±šŗ¬ÓŠ0.4molµÄC-C¼üÓė0.4mol µÄSi-O ¼ü
D.³£ĪĀĻĀ£¬ĻņNH4ClČÜŅŗÖŠ¼ÓČėÉŁĮæNaOH¹ĢĢå£ØČÜŅŗĪĀ¶Čƻӊ±ä»Æ£©£¬ČÜŅŗÖŠ![]() µÄÖµŌö“ó
µÄÖµŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŹµŃéŹŅÖŠÓƶžŃõ»ÆĆĢøśÅØŃĪĖį·“Ó¦ÖʱøøÉŌļ“æ¾»µÄĀČĘų”£ĖłÓĆŅĒĘ÷ČēĶ¼£ŗ
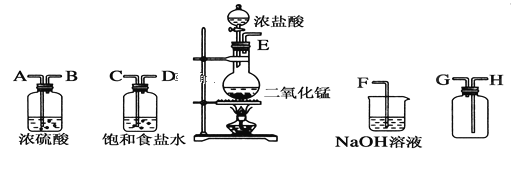
£Ø1£©Į¬½ÓÉĻŹöŅĒĘ÷µÄÕżČ·Ė³Šņ(Ģīø÷½ÓæŚ“¦µÄ×ÖÄø)£ŗ__½Ó__£»__½Ó__£»__½Ó__£»__½Ó__”£
£Ø2£©×°ÖĆÖŠ£¬±„ŗĶŹ³ŃĪĖ®µÄ×÷ÓĆŹĒ______________£»NaOHČÜŅŗµÄ×÷ÓĆŹĒ____________”£
£Ø3£©¢ŁĘųĢå·¢Éś×°ÖĆÖŠ½ųŠŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_____________________________£»øĆ·½³ĢŹ½ÖŠĢåĻÖÅØŃĪĖįµÄ__________________”¢____________________ ŠŌÖŹ£»Ńõ»Æ¼ĮŗĶ»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±Č£ŗ________________________________________£»
¢ŚNaOHČÜŅŗÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_______________________________________£»
£Ø4£©ŹµŃéŹŅÓĆĻĀĮŠ·½·ØÖĘČ”ĀČĘų£ŗ¢ŁÓĆŗ¬4 mol ĀČ»ÆĒāµÄÅØŃĪĖįÓė×ćĮæµÄ¶žŃõ»ÆĆĢ·“Ó¦£»¢ŚÓĆ87 g ¶žŃõ»ÆĆĢÓė×ćĮæÅØŃĪĖį·“Ó¦£¬Čō²»æ¼ĀĒĀČ»ÆĒāµÄ»Ó·¢£¬Ōņ·“Ó¦ŗóĖłµĆĀČĘųµÄĪļÖŹµÄĮæ£Ø_____£©
A£®¢Ł±Č¢Ś¶ą B£®¢Ś±Č¢Ł¶ą C£®Į½ÖÖ·½·ØŅ»Ńł¶ą D£®ĪŽ·Ø±Č½Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬·“Ó¦N2(g)+3H2(g)![]() 2NH3(g)“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ
2NH3(g)“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ
A. c(N2):c(H2):c(NH3)=1:3:2
B. N2”¢H2ŗĶNH3µÄĪļÖŹµÄĮæ·ÖŹż²»ŌŁøıä
C. N2ÓėH2µÄĪļÖŹµÄĮæÖ®ŗĶŹĒNH3µÄĪļÖŹµÄĮæµÄ2±¶
D. µ„Ī»Ź±¼äĄļĆæŌö¼ÓlmolN2£¬Ķ¬Ź±Ōö¼Ó3molH2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČ”100.0 mLNa2CO3ŗĶNa2SO4µÄ»ģŗĻČÜŅŗ£¬¼ÓČė¹żĮæBaCl2ČÜŅŗŗóµĆµ½16.84g³Įµķ£¬ÓĆ¹żĮæĻ”ĻõĖį“¦Ąķŗó³ĮµķÖŹĮæ¼õÉŁÖĮ6.99g,Ķ¬Ź±ČÜŅŗÖŠÓŠĘųÅŻ²śÉś”£ŹŌĒó£ŗ
£Ø1£©Ō»ģŗĻŅŗÖŠNa2SO4µÄĪļÖŹµÄĮæÅضČĪŖ_____£»
£Ø2£©²śÉśµÄĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ¶ąÉŁ__________£æ£ØŅŖĒ󊓳ö¼ĘĖć¹ż³Ģ£¬Ö»Š“½į¹ū²»øų·Ö£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚŠĀÖĘĀČĖ®µÄŠšŹöÕżČ·µÄŹĒ( )
A.¹āÕÕŠĀÖĘĀČĖ®ÓŠĘųÅŻŅŻ³ö£¬øĆĘųĢåŹĒCl2B.ŠĀÖĘĀČĖ®·ÅÖĆŹżĢģŗóĖįŠŌ¼õČõ
C.ŠĀÖĘĀČĖ®ÖŠÖ»ŗ¬ÓŠCl2ŗĶH2OĮ½ÖÖ·Ö×ÓD.ŠĀÖĘĀČĖ®æÉŹ¹Ą¶É«ŹÆČļŹŌÖ½ĻȱäŗģŗóĶŹÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬Ļņ20.00mL 0.200 0 mol/LNH4ClČÜŅŗÖŠÖšµĪ¼ÓČė0.2000 mol/LNaOHČÜŅŗŹ±£¬ČÜŅŗµÄpHÓėĖł¼ÓNaOHČÜŅŗĢå»żµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£Ø²»æ¼ĀĒ»Ó·¢£©”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
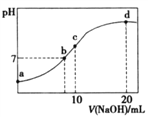
A. aµćČÜŅŗÖŠ£ŗc(H+)+c(NH3”¤H2O)=c(OH-)+c(NH4+)
B. bµćČÜŅŗÖŠ£ŗc(Cl-)=c(Na+)>c(H+)=c(OH-)
C. cµćČÜŅŗÖŠ£ŗc(NH3”¤H2O)+ c(NH4+)= c(Cl-)+ c(OH-)
D. dµćČÜŅŗÖŠ£ŗc(Cl-)> c(NH3”¤H2O)> c(OH-)> c(NH4+)
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com