
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。

(1)装置A中发生反应的离子方程式为_____________________________。
(2)该实验装置明显存在不足之处,改进的措施为____________________
(3)已知在装置C中通入一定量的氯气后,观察到测得D中有黄红色的气体(提示:是一种氯的氧化物)。已知C中所得固体含有NaHCO3。现对C中的成分进行猜想和探究。
①提出合理假设.
假设一:存在两种成分,为NaHCO3、NaCl
假设二:存在三种成分,为NaHCO3、Na2CO3、NaCl
②设计方案并实验.请在表格中写出实验步骤以及预期现象和结论.
限选试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。

结论:由步骤3的结论结合步骤2中的a,则假设一成立;由步骤3的结论结合步骤2中的b,则假设二成立.
若C中有0.1molCl2恰好与10.6gNa2CO3反应,且假设一成立,由此可推知C中反应生成的氯的氧化物为
(写化学式),写出C中发生反应的化学方程式 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届江汉油田海南海政学校高三月考化学试卷(解析版) 题型:填空题
(两个选项符合题意,6分)下列数据是对应物质的熔点,有关的判断错误的是( )
Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
920 ℃ | 97.8 ℃ | 1291 ℃ | 190 ℃ | 2073 ℃ | -107 ℃ | -57 ℃ | 1723 ℃ |
A.只要含有金属阳离子的晶体就一定是离子晶体
B.在共价化合物中各原子都形成8电子结构
C.同族元素的氧化物可形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
19-II(14分)如图为几种晶体或晶胞的构型示意图。

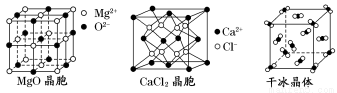
请回答下列问题:
(1)这些晶体中,粒子之间以共价键结合形成的晶体是____________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_________________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能________(填“大于”或“小于”)MgO晶体的晶格能,原因是_______________。
(4)每个铜晶胞中实际占有________个铜原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰,除因为H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_________。
查看答案和解析>>
科目:高中化学 来源:2016届河南省郑州市新高三年级调研检测化学试卷(解析版) 题型:填空题
(14分)I.元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3 :4,且M原子的质子数是Y原子的2倍;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)写出Y、Z、N按原子个数之比1 :1:1形成的化合物的电子式_______________。
(2)写出由X、Y、Z、M、N中某些原子形成的18电子分子和18电子离子发生氧化还原反应的离子方程式:_________________。
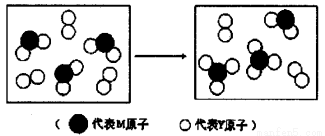
(3)上图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:________________。
Ⅱ.A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA2、BA3的型分子。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。请回答下列问题:
(4)D元素在元素周期表中的位置是_____________。
(5)B与D所形成的化合物的化学键类型为______________。
(6)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的离子方程式为_____________。
(7)实验室里除去BA2气体,可用下列试剂中的_____________(填字母)。
A.酸性高锰酸钾溶液 B.浓硫酸
C.NaOH溶液 D.NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上学期升学化学试卷(解析版) 题型:填空题
(14分)五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。D周期序数等于D原子最外层电子数。E原子半径是同周期中最小的(除稀有气体外)根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是 (用元素符号填写),其中D的最高价氧化物是 氧化物。
(2)乙物质中存在的化学键类型是 。
(3)化合物乙的电子式 。
(4)写出C与D的最高价氧化物对应的水化物反应的离子方程式 。
(5)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的主要成分的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三9月调考化学试卷(解析版) 题型:选择题
还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:

已知转化过程中的反应为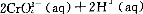
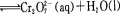
转化后所得溶液中铬元素的含量为28.6 g/L, CrO42-有10/11转化为Cr2072-,下列说法不正确的是
A.溶液颜色保持不变,说明上述可逆反应达到平衡状态
B.若用绿矾(FeS04·7H2O)作还原剂,处理1 L废水,至少需要458.7g
C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5
D.常温下Ksp=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上第三次月考化学试卷(解析版) 题型:选择题
实验室常利用以下反应制取少量氮气:NaNO2 + NH4Cl = NaCl + N2↑ + H2O
关于该反应的下列说法不正确的是
A.NaNO2的氧化性大于N2
B.每生成1molN2,转移的电子数的物质的量为6mol
C.NH4Cl的还原性大于N2
D.氮元素既被氧化又被还原
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上第三次月考化学试卷(解析版) 题型:选择题
下列化学实验事实及其结论都正确的是
选项 | 实验事实 | 结论 |
A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
下图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是
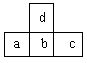
A. a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a
B. d的氢化物比b的氢化物稳定
C. d与c不能形成化合物
D. 原子半径的大小顺序是a>b>c>d
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
常温下,下列溶液中的微粒浓度关系正确的是
A.新制氯水中加入固体NaOH: c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3—)>c(CO32—)>c(H2CO3)
C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH+4)>c(OH-)=c(H+)
D.0.2mol·L-1CH3COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c (CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com