
(1)此次闪电所产生的NO的物质的量有多大?
(2)此次雷雨闪电的生成物相当于给土壤施了多少尿素?
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:物理教研室 题型:038
氮肥是广泛使用的肥料,请结合有关材料,回答问题.
(1)硫酸铵是农村常用的一种铵态氮肥.
①硫酸铵中氮的质量分数是__________.
②实验测得某硫酸铵肥料中氮元素的质量分数为20%,则该样品中可能混有_____________.
[ ]
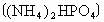
(2)电闪雷鸣是日常生活中司空见惯的现象.在闪电发生的过程中,空气中的氮气和氧气直接化合.假设某次雷电放出的能量为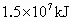 ,已知
,已知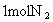 和
和 化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
①此次闪电所产生的NO的物质的量是_____mol.
②此次雷电的生成物相当于给土壤施加了_______千克的尿素化肥〔尿素化学式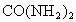 〕.
〕.
查看答案和解析>>
科目:高中化学 来源: 题型:058
氮肥是广泛使用的肥料,请结合有关材料,回答问题.
(1)硫酸铵是农村常用的一种铵态氮肥.
①硫酸铵中氮的质量分数是__________.
②实验测得某硫酸铵肥料中氮元素的质量分数为20%,则该样品中可能混有_____________.
[ ]
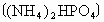
(2)电闪雷鸣是日常生活中司空见惯的现象.在闪电发生的过程中,空气中的氮气和氧气直接化合.假设某次雷电放出的能量为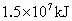 ,已知
,已知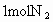 和
和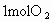 化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
化合时要吸收181kJ能量,闪电时有1/1000的能量用于这一反应.
①此次闪电所产生的NO的物质的量是_____mol.
②此次雷电的生成物相当于给土壤施加了_______千克的尿素化肥〔尿素化学式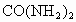 〕.
〕.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)此次闪电所产生的NO的物质的量有多大?
(2)此次雷雨闪电的生成物相当于给土壤施了多少千克尿素?
查看答案和解析>>
科目:高中化学 来源: 题型:
电闪雷鸣是日常生活中司空见惯的现象。设某次雷电中,两块云团间的电势差约为109 V,放电荷量约为15 C。在闪电过程中,空气中的氮气和氧气直接化合,已知每摩尔氧气和氮气化合要吸收180.74 kJ的能量,闪电时有千分之一的能量用于这一反应,那么:
(1)此次闪电所产生的NO的物质的量有多大?
(2)此次雷雨闪电的生成物相当于给土壤施了多少千克尿素?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com