
| A. | 酸根中可能含有氧元素 | B. | 正盐中一定不含氢元素 | ||
| C. | 碱中一定含有氢元素和氧元素 | D. | 酸式盐中含有氢元素 |
分析 酸是指在电离时产生的阳离子全部是氢离子的化合物;碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;盐是由金属离子(或铵根离子)和酸根离子组成的化合物,酸式盐是多元酸和碱部分反应得到的盐,据此进行分析判断即可.
解答 解:A、酸是电离时电离出的阳离子全部是氢离子的化合物,酸中可能有氧,例如硫酸,故A正确;
B、盐是由金属阳离子(铵根离子)和酸根阴离子组成的化合物,盐中不一定含有氢元素,如NaCl,故B错误;
C、碱是电离时电离出的阴离子全部是氢氧根离子的化合物,故碱中一定含的氢元素,故C正确;
D、酸是电离时电离出的阳离子全部是氢离子的化合物,酸式盐是多元酸和碱部分反应生成,故酸式盐中一定含氢元素,故D正确;
故选B.
点评 本题难度不大,掌握酸、碱、盐的概念、特征并能灵活运用即可正确解答本题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 粗硅$→_{高温}^{氯气}$ SiCl4 $→_{高温}^{氢气}$Si | |
| B. | Mg(OH)2 $\stackrel{盐酸}{→}$ MgCl2(aq)$\stackrel{电解}{→}$ Mg | |
| C. | Fe2O3 $\stackrel{盐酸}{→}$ FeCl3(aq)$\stackrel{蒸发}{→}$ 无水FeCl3 | |
| D. | AgNO3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$→_{加热}^{蔗糖}$ Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
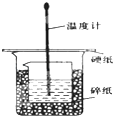 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如 图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如 图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为正极,碳为负极 | |
| B. | 负极反应为2NH4++2e-═2NH3↑+H2↑ | |
| C. | 工作时电子由碳极经外电路流向锌极 | |
| D. | 长时间连续使用时,内装的糊状物可能流出腐蚀电器 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe粉(硫粉) | B. | Na2CO3粉末(NaHCO3) | ||
| C. | NaCl(碘) | D. | KMnO4(MnO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4 •5H2O、磁性氧化物都是纯净物 | |
| B. | 一种物质不是电解质就是非电解质 | |
| C. | 稀硫酸、NaCl溶液是实验室常见的电解质 | |
| D. | 二氧化硫可广泛用于食品的增白 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| N2(g) | + | 3H2(g) | ? | 2NH3 | |
| ① | 1mol | 3mol | 0mol | ||
| ② | 0mol | 0mol | 2mol | ||
| ③ | 0.5mol | 1.5mol | 1mol | ||
| ④ | 1mol | 3mol | 2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com