
 ��ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ģ���ͼΪN2��g����O2��g����Ӧ����NO��g�������е������仯������˵������ȷ���ǣ�������
��ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ģ���ͼΪN2��g����O2��g����Ӧ����NO��g�������е������仯������˵������ȷ���ǣ�������| A�� | 1mo N2��g����1mo O2��g����ȫ��Ӧ�ų�������Ϊ180kJ | |
| B�� | ͨ������£�N2��g����O2��g�������ֱ������NO | |
| C�� | 1mol N2��g����1molO2��g�������������2molN��g����������� | |
| D�� | NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ |
���� A�����������仯���������ԭ�ӣ����ݷ�Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų������������жϣ�
B�������������ڷŵ��������ܷ�Ӧ��
C������A������ʱ��жϷ�Ӧ�����仯����Ϸ�Ӧǰ�������غ������
D��һ���������ܺ��������Ʒ�Ӧ��
��� �⣺A���ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų���������N2+O2�T2NO����H=946kJ/mol+498kJ/mol-2��632kJ/mol=+180kJ/mol����Ӧ�����ȷ�Ӧ����A����
B��ͨ������£�N2��g����O2��g����ϲ���ֱ������NO����Ҫ�ŵ���������B����
C����ͼ�����ݿɵ÷�Ӧ����Ķ������գ�946+498��=1444kJ/mol������������������γɷų�2��632=1264 kJ/mol���������ʸ÷�Ӧ�����ȷ�Ӧ�����������غ㣬1 mol N2��g����1 mol O2��g�����е�������С��2 mol NO��g�����е�����������C��ȷ��
D��һ���������ܺ��������Ʒ�Ӧ�����������������D����
��ѡ��C��
���� ������Ҫ�����˷�Ӧ�����仯�ļ�����жϣ���Ӧ���ʱ���㷽���������غ��ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ӳɡ���ȥ��ȡ�� | B�� | ��ȥ���ӳɡ���ȥ | C�� | ��ȥ���ӳɡ�ȡ�� | D�� | ȡ������ȥ���ӳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4L | B�� | 6L | C�� | 8L | D�� | 12L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�11.2L�������еķ�֮��Ϊ0.5NA | |
| B�� | ���³�ѹ�£�1mol�������е�������Ϊ7NA | |
| C�� | �ڱ�״̬�£�22.4LH2O���е�ԭ����ĿΪ3NA | |
| D�� | 32gO2����ԭ����ĿΪ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2��NaOH��Һ | B�� | NO2��ˮ | C�� | NH3��ˮ | D�� | Cl2��NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
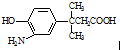 �ı�������ȷ���ǣ�������
�ı�������ȷ���ǣ�������| A�� | �������ܷ������۷�Ӧ | |
| B�� | ��������7�ֲ�ͬ��������ԭ�� | |
| C�� | ��������FeCl3��Һ��ɫ��1mol������������뺬1mol Br2����ˮ����ȡ����Ӧ | |
| D�� | 1 mol�������������Na��NaOH��NaHCO3�����ʵ���֮��Ϊ2��2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
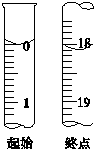 �ⶨ��Ʒ����
�ⶨ��Ʒ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ��pHС��7 | B�� | c��CH3COOH��+c��CH3COO-��=0.20 mol•L-1 | ||
| C�� | c��CH3COO-��+c��OH-��=0.10 mol•L-1 | D�� | c��CH3COOH����c��CH3COO-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com