
| A. | Na2O2中氧元素化合价为-1 | |
| B. | Na2O2能与水反应,所以Na2O2可以作气体的干燥剂 | |
| C. | Na2O2与水反应时,Na2O2是氧化剂,水是还原性 | |
| D. | Na2O2与二氧化碳反应时,Na2O2只作氧化剂 |
分析 A、Na2O2中Na元素为+1价,根据化合价的代数和为0分析;
B、过氧化钠与水反应生成氧气;
C、Na2O2与水反应时,只有Na2O2中O元素发生化合价的变化;
D、Na2O2与二氧化碳反应时,只有Na2O2中O元素发生化合价的变化.
解答 解:A.Na2O2中Na元素为+1价,根据化合价的代数和为0可知,氧元素化合价为-1,故A正确;
B.过氧化钠与水反应生成氧气,会在气体中引入杂质,所以Na2O2不可以作气体的干燥剂,故B错误;
C.Na2O2与水反应时,只有Na2O2中O元素发生化合价的变化,所以过氧化钠既是还原剂又是氧化剂,故C错误;
D.Na2O2与二氧化碳反应时,只有Na2O2中O元素发生化合价的变化,所以过氧化钠既是还原剂又是氧化剂,故D错误;
故选A.
点评 本题考查钠的重要化合物知识,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握过氧化钠与水、二氧化碳反应的特点,学习中注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下11.2LO2和16gO3中含有的O数均为 NA | |
| B. | 32g氧气所含质子数为NA | |
| C. | 1mol/L的CaCl2溶液中含有的Cl-为2NA | |
| D. | 12.6g水所含电子数目为0.7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液中滴加过量Na2S溶液:2Fe3++S2-═2Fe2++S↓ | |
| B. | 将Na2O2固体投入H218O中:2Na2O2+2H218O═4Na++4OH-+18O2↑ | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| D. | 少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O═2C6H5OH+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
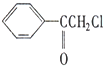 中国是《日内瓦协定书》的缔约国,反对使用化学武器,反对任何形式的化学武器扩散.苯氯乙酮是一种具有荷花香味且有强催泪作用的杀伤性化学毒剂,它的结构简式为:
中国是《日内瓦协定书》的缔约国,反对使用化学武器,反对任何形式的化学武器扩散.苯氯乙酮是一种具有荷花香味且有强催泪作用的杀伤性化学毒剂,它的结构简式为: 、
、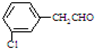 、
、 、
、 、还有
、还有 或
或 (任写一个合理结构).
(任写一个合理结构). 与溴水充分反应,需消耗4mol单质溴;
与溴水充分反应,需消耗4mol单质溴; 与氢气完全加成后的产物的结构简式
与氢气完全加成后的产物的结构简式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C14H18O5 | B. | C14H16O4 | C. | C16H22O5 | D. | C16H20O5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com