
【题目】常温下,用0.1000mol·L-1 NaOH溶液滴定20.00mL 0.1000 mol·L-1某酸(HA)溶液,溶液中HA、A-的物质的量分数δ(X)随pH的变化如图所示。[已知δ(X)=![]() ]下列说法正确的是
]下列说法正确的是
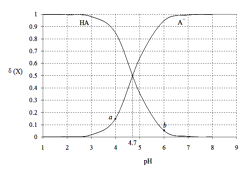
A.Ka(HA)的数量级为10-5
B.溶液中由水电离出的c(H+):a点>b点
C.当pH=4.7时,c(A-)+c(OH-)=c(HA)+c(H+)
D.当pH=7时,消耗NaOH溶液的体积为20.00mL
科目:高中化学 来源: 题型:
【题目】镁电池作为一种低成本、高安全的储能装置,正受到国内外广大科研人员的关注。一种以固态含Mg2+的化合物为电解质的镁电池的总反应如下。下列说法错误的是
xMg+V2O5 ![]() MgxV2O5
MgxV2O5
A. 充电时,阳极质量减小
B. 充电时,阴极反应式:Mg2++2e-=Mg
C. 放电时,正极反应式为:V2O5+xMg2++2xe-=MgxV2O5
D. 放电时,电路中每流过2mol电子,固体电解质中有2molMg2+迁移至正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法中,正确的是
A.容量瓶、滴定管、分液漏斗使用前都要检查是否漏液
B.配制1.00![]() 和4%的NaOH溶液,所用实验用品完全相同
和4%的NaOH溶液,所用实验用品完全相同
C.用稀硫酸溶液洗涤并灼烧铂丝后,再进行焰色反应
D.用广泛pH试纸测得0.10![]() NaHCO3溶液的
NaHCO3溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是五种由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的不同的阴阳离子组成,且均易溶于水的物质,分别取它们的水溶液进行实验,现象如下:
中的不同的阴阳离子组成,且均易溶于水的物质,分别取它们的水溶液进行实验,现象如下:
①分别向五种溶液中加入稀盐酸,C、E均有气泡产生,且E的液面上出现红棕色气体
②C、D混合时,剧烈反应,同时产生白色沉淀和大量气体;A、C混合时,仅有刺激性气味气体产生
③少量A与D混合时,产生白色沉淀,过量A与D混合时,无现象
回答下列问题:
(1)实验①,C中产生的气体是________________(填化学式)。
(2)物质A、D的化学式分别是_____________,________________。
(3)C、D混合时发生反应的离子方程式是__________________________。
(4)将A、E的溶液在烧杯中混合,其现象是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为电解饱和食盐水的实验装置。据此,下列叙述不正确的是 ( )
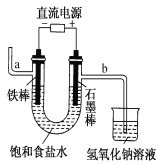
A.装置中a管能产生氢气
B.b管导出的是能使湿润的淀粉碘化钾试纸变蓝的气体
C.在石墨棒电极区域有NaOH生成
D.以电解饱和食盐水为基础制取氯气等产品的工业称为“氯碱工业”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为________,X的相对原子质量为________。
(2)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mL O2和10mL F2,则A的化学式为________。
(3)有X、Y、Z三种元素, X原子核内无中子, Y原子的第三个电子层上有2个电子, Z原子最外层电子数是其电子层数的3倍。试画出Y原子结构示意图______________。这三种元素所组成的化合物的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
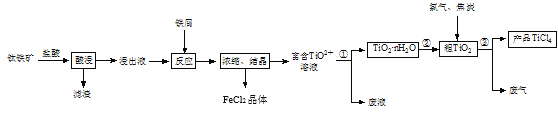
【题目】四氯化钛(TiCl4)是制取航空材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3,不溶于水)制备TiCl4等产品的一种工艺流程示意如图:
回答下列问题:
(1)“酸浸”时需要将钛铁矿粉碎,其目的是____。
(2)浸出液呈强酸性,含有TiO2+、Fe2+及少量Fe3+、Al3+等离子,则生成TiO2+的离子方程式是__。
(3)“反应”时需加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是____。
(4)通过控制条件,可以使过程①中生成的TiO2·nH2O形成一种液态分散系,用一束光照射该分散系能够产生丁达尔效应,则分散质颗粒直径的范围是____。
(5)过程①制得的固体TiO2·nH2O需用过量酸清洗以除去其中的Fe(OH)3杂质,检验Fe(OH)3杂质除净的实验方法是____。
(6)过程③生成的废气中含有CO,则TiO2和焦炭、氯气在高温下发生反应的化学方程式是___。
(7)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是____(只要求写出一项)。
(8)依据表中信息,可采用___方法精制含少量SiCl4杂质的TiCl4。
TiCl4 | SiCl4 | |
熔点/℃ | -25.0 | -68.8 |
沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() ,下列有机物能够合成
,下列有机物能够合成![]() 的组合是( )
的组合是( )
①1,3-丁二烯 ②2-甲基-l,3-丁二烯 ③1,3-戊二烯 ④2,3-二甲基-l,3-丁二烯
⑤2,3-二甲基-l,3-戊二烯 ⑥乙炔 ⑦丙炔 ⑧2-丁炔
A. ①、⑦及④、⑧ B. ⑤、⑥及③、⑧
C. ①、③及②、⑧ D. ②、⑧及④、⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)48g氧气和48g臭氧(O3),它们所含的原子数_______ (填“相同”或“不同”,它们在同温同压下的体积比是________。0.2 mol NH3分子与________个CH4含有的电子数相同,与_______g H2O含有的氢原子数相同,与标准状况下____ L CO含有的原子数相等。
(2)483g Na2SO4·10H2O中所含的Na2SO4·10H2O的物质的量是_______; Na2SO4·10H2O的摩尔质量是________,所含Na+的物质的量是________。含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是________。
(3)实验室常用的浓盐酸密度为1.17 g·mL-1,质量分数为36.5 %。
①此浓盐酸的物质的量浓度为__________________。
②取此浓盐酸50mL,用蒸馏水稀释为200mL,稀释后盐酸的物质的量浓度为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com