
| A. | 若三种溶液中c(H+)分别为a1 mol•L-1、a2 mol•L-1、a3 mol•L-1,则它们的大小关系为$\frac{1}{2}$a2=a1=a3 | |
| B. | 等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为b1 mol、b2 mol、b3 mol,则它们的大小关系为b1=b2<b3 | |
| C. | 分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为V1=V2=V3 | |
| D. | 分别与Zn反应,开始时生成H2的速率分别为v1、v2、v3,其大小关系为v2>v1>v3 |
分析 A.醋酸的弱电解质,部分电离,硫酸是二元强酸、盐酸是一元强酸,据此判断氢离子浓度大小;
B.生成盐的物质的量与酸的物质的量相等;
C.中和一定量NaOH溶液生成正盐时,酸的浓度相等时,如果是一元酸,所用酸的体积相等,如果是二元酸,酸的体积是一元酸的一半;
D.生成氢气的反应速率与氢离子浓度成正比.
解答 解:A.醋酸的弱电解质,部分电离,硫酸是二元强酸、盐酸是一元强酸,物质的量浓度相等的三种酸,氢离子浓度大小是a2=2a1>a3,故A错误;
B.根据原子守恒知,生成盐的物质的量与酸的物质的量相等,所以生成盐的物质的量关系为:b1=b2=b3,故B错误;
C.中和一定量NaOH溶液生成正盐时,酸的浓度相等,如果是一元酸,所用酸的体积相等,如果是二元酸,酸的体积是一元酸的一半,所以三种酸的体积大小关系是V1=2V2=V3,故C错误;
D.生成氢气的反应速率与氢离子浓度成正比,根据(1)中氢离子浓度大小顺序是a2=2a1>a3,所以反应速率大小顺序是υ2>υ1>υ3,故D正确.
故选D.
点评 本题考查了弱电解质的电离,为高频考点,难度不大,注意D中生成氢气的反应速率与氢离子浓度成正比,分清是初始速率还反应过程中的反应速率,注意反应速率与氢离子浓度有关,与电解质强弱无关,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 将30 mL 0.5 mol/L NaOH溶液加水稀释到500 mL,所得溶液的NaOH的浓度为0.3 mol/L | |
| B. | 配制250 mL 1.0 mol/L H2SO4溶液,需要18 mol/L的浓H2SO4的体积约为13.9 mL | |
| C. | 0.270 kg质量分数为10%的CuCl2溶液中Cl-的物质的量为0.2 mol | |
| D. | 80 g NaOH溶于1 L水中所得的溶液的物质的量浓度为2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
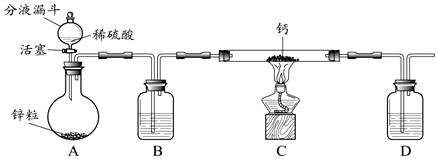
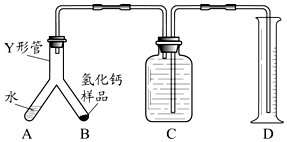
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
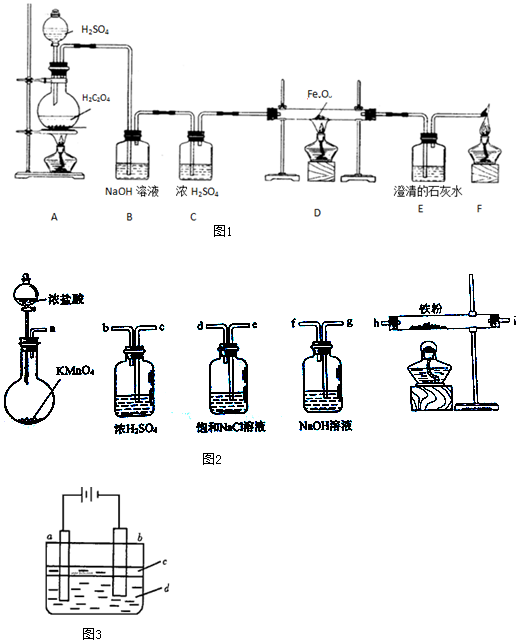
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
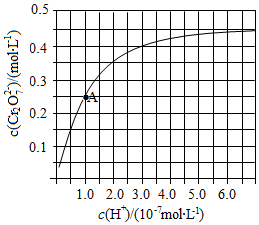 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba( NO3-)2=Ba2++( NO3-) 2 | B. | NaHSO4=Na++H++SO42- | ||
| C. | H2SO4=2H++SO42- | D. | KClO3=K++ClO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 这个反应是氧化还原反应 | B. | 制造过程中元素种类发生改变 | ||
| C. | 另一种化合物为NaCl | D. | 金刚石属于金属单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com