
已知常温下在溶液中可发生如下两个离子反应:
Ce4++Fe2+===Fe3++Ce3+
Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是 ( )
A.Sn2+、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ce3+
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
下列物质在指定条件下电离方程式正确的是 ( )
A.Na2CO3溶于水 Na2CO3===Na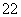 +CO
+CO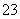
B.Al(OH)3酸式电离 Al(OH)3===H++AlO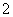 +H2O
+H2O
C.NaHS溶于水HS-的电离 HS-+H2O H2S+OH-
H2S+OH-
D.NaHCO3加热熔化 NaHCO3===Na++HCO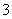
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下;下列各组离子在指定溶液中一定能大量共存的是( )。
A.0.1 mol·L-1 NaOH溶液:K+、Na+、S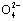 、C
、C
B.0.1 mol·L-1 Na2CO3溶液:K+、Ba2+、N 、Cl-
、Cl-
C.0.1 mol·L-1 FeCl3溶液:K+、N 、I-、SCN-
、I-、SCN-
D.c(H+) /c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、N
/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、N
查看答案和解析>>
科目:高中化学 来源: 题型:
酒后驾车。这时酒精(CH3CH2OH)被K2Cr2O7氧化为醋酸(CH3COOH)。该氧化还原反应的方程式可表示为:2K2Cr2O7+3CH3CH2OH+8H2SO4→2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O ;在这一反应中,氧化剂是  ,还原剂________,氧化产物是 ,还原产物是 。
,还原剂________,氧化产物是 ,还原产物是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
NaClO2可用作造纸的漂白剂,它由H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2制得,下列说法正确的是
A.H2O2是氧化剂,H2O2中的氧元素被还原
B.每生成1 mol O2转移的电子的物质的量为4 mol
C.ClO2中的氯元素被氧化
D.ClO2是氧化剂,H2O2是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既是离子反应,又是氧化还原反应的是( )
A.BaCl2溶液中滴加稀H2SO4
B.盐酸和氧化铁反应
C.铁片放入CuSO4溶液中
D.氢气还原CuO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.元素由化合态变成游离态时,它可能被氧化,也可能被还原
C.元素的原子得失电子后,一定形成8电子的稳定结构
D.有单质参加或生成的反应一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
己知:Ksp[Fe(OH)3]= 4.0×10-38
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为 :
(2)过程I 加入铁屑的主要作用是 ,分离得到固体的主要成分是 ,从固体中分离出铜需采用的方法是 ;
(3)过程II中发生反应的化学方程式为 ;
(4)过程II中调节溶液的pH为5,金属离子浓度为 。(列式计算)
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C4H10O的醇能被氧化,但氧化产物不是醛,则该醇的结构简式是 ( )
A.C(CH3)3OH B.CH3CH2CH(OH)CH3
C.CH3CH2CH2CH2OH D.CH3CH(CH3)CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com