
分析 (1)气体的摩尔质量与标况下的密度关系为:M=ρ×22.4L/mol,据此计算出该烃的摩尔质量;再根据该烃中C、H的质量分数计算出其分子式、实验式;
(2)根据(1)的计算结果写出该烃的分子式;
(3)根据“经红外光谱测定该烃分子中含一个双键”及该烃的分子式写出该烃可能的结构简式及名称.
解答 解:(1)该烃的摩尔质量为:M=2.5g/L×22.4L/mol=56g/mol,
该烃分子中含有的碳原子数为:$\frac{56×85.7%}{12}$≈4,含有的氢原子数为:$\frac{56-12×4}{1}$=8,
该烃的分子式为:C4H8,则该烃的实验式为CH2,
答:该烃的实验式为CH2;
(2)根据(1)可知,该烃的分子式为C4H8,
答:该烃的分子式为C4H8;
(3)经红外光谱测定该烃分子中含一个双键,该烃分子中含有1个碳碳双键,该烃为丁烯,分子式为C4H8且属于烯烃的有机物结构有3种:1-丁烯 CH2=CHCH2CH3、2-丁烯 CH3CH=CHCH3、2-甲基-1-丙烯 CH2=C(CH3)2,
答:该烃的各种同分异构体的结构简式及名称为:1-丁烯 CH2=CHCH2CH3、2-丁烯 CH3CH=CHCH3、2-甲基-1-丙烯 CH2=C(CH3)2.
点评 本题考查了有机物分子式的计算、同分异构体的书写,题目难度中等,注意掌握常见有机物结构与性质,明确计算有机物分子式的方法,能够正确书写常见有机物的同分异构体.


 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe、Cu、Zn原子最外层电子数依次增多 | |
| B. | N、O、F元素最高正化合价依次升高 | |
| C. | P、S、Cl第一电离能依次增大 | |
| D. | Na、K、Rb的金属性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
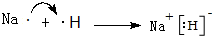 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,B的结构简式
,B的结构简式 或
或 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ②③④⑤ | C. | 只有① | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;Na2HPO4的电离方程式为Na2HPO4=2Na++HPO42-.
;Na2HPO4的电离方程式为Na2HPO4=2Na++HPO42-.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
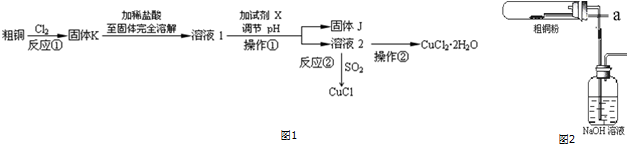
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
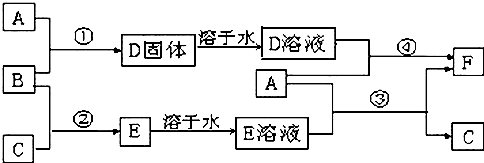
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com