
【题目】(1)下列各组粒子互为同位素的是 (填编号,下同)。互为同素异形体的是 ,互为同分异构体的是 互为同系物的是 。
①16O2和18O3
②质子数相同而中子数不同的两种粒子
③11H、D、T
④3015R和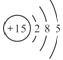 (核内15个中子)
(核内15个中子)
⑤葡萄糖和果糖
⑥
⑦CH3CH2CH2CH2CH2CH3和(CH3)2CHCH(CH3)2
⑧(CH3)2CHCH(CH3)2和C(CH3)4
(2)生活中的一些问题常涉及化学知识,下列叙述正确的是(填序号) 。
①淀粉、蛋白质都是天然有机高分子化合物
②食用植物油的重要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质
③禁止使用含铅汽油是为了提高汽油的燃烧效率
④福尔马林是一种良好的杀毒剂,也可用来消毒自来水
⑤随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常放入生石灰
⑥向蛋白质溶液中加入(NH4)2SO4浓溶液,蛋白质会析出,加水后不再溶解
⑦为保证加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
(3)在实验室生成乙酸乙酯的可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) .
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
【答案】
(1)③;①;⑤⑦;⑧ ;
(2)①②;
(3)②④⑤。
【解析】
试题分析:(1)①16O2和18O3是同种元素形成的不同单质,互为同素异形体;②质子数相同而中子数不同的两种粒子,若为分子,则不是同位素;③11H、D、T具有相同质子数,不同中子数同一元素的不同原子,互为同位素;④3015R和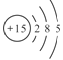 (核内15个中子)质子数和中子数都相同,属于同种核素;⑤葡萄糖和果糖是具有相同分子式,结构不同的化合物,互为同分异构体;⑥
(核内15个中子)质子数和中子数都相同,属于同种核素;⑤葡萄糖和果糖是具有相同分子式,结构不同的化合物,互为同分异构体;⑥ 分子式相同,结构相同,属于同种物质;CH3CH2CH2CH2CH2CH3和(CH3)2CHCH(CH3)2分子式相同结构不同,二者互称同分异构体;⑧(CH3)2CHCH(CH3)2和C(CH3)4结构相似,在分子组成上相差一个CH2原子团,互称同系物。所以互为同位素的是③。互为同素异形体的是①;互为同分异构体的是⑤⑦;互为同系物的是⑧;(2)①淀粉、蛋白质都是天然有机高分子化合物,正确;②食用植物油的重要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质,正确;③铅是重金属,对人体有害,禁止使用含铅汽油是为了防止造成环境污染,错误;④福尔马林有毒,不可用来消毒自来水,错误;⑤生石灰和水反应生成氢氧化钙,吸收水分,不是作还原剂的作用,错误;⑥向蛋白质溶液中加入(NH4)2SO4浓溶液,蛋白质会发生盐析而析出,加水后物质可以再溶解,错误;⑦酶是蛋白质,高温易变性,用沸水溶解洗衣粉,会使酶失去活性,错误。故正确的为:①②;(3) ①单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,错误;②单位时间里,生成1mol乙酸乙酯表示正反应速率,生成1mol乙酸表示逆反应速率,等于化学计量数之比,说明到达平衡,正确;③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,错误;④正反应的速率与逆反应的速率相等,说明到达平衡状态,正确;⑤混合物中各物质的浓度不再变化,反应到达平衡状态,正确。故正确的是②④⑤。
分子式相同,结构相同,属于同种物质;CH3CH2CH2CH2CH2CH3和(CH3)2CHCH(CH3)2分子式相同结构不同,二者互称同分异构体;⑧(CH3)2CHCH(CH3)2和C(CH3)4结构相似,在分子组成上相差一个CH2原子团,互称同系物。所以互为同位素的是③。互为同素异形体的是①;互为同分异构体的是⑤⑦;互为同系物的是⑧;(2)①淀粉、蛋白质都是天然有机高分子化合物,正确;②食用植物油的重要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质,正确;③铅是重金属,对人体有害,禁止使用含铅汽油是为了防止造成环境污染,错误;④福尔马林有毒,不可用来消毒自来水,错误;⑤生石灰和水反应生成氢氧化钙,吸收水分,不是作还原剂的作用,错误;⑥向蛋白质溶液中加入(NH4)2SO4浓溶液,蛋白质会发生盐析而析出,加水后物质可以再溶解,错误;⑦酶是蛋白质,高温易变性,用沸水溶解洗衣粉,会使酶失去活性,错误。故正确的为:①②;(3) ①单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,错误;②单位时间里,生成1mol乙酸乙酯表示正反应速率,生成1mol乙酸表示逆反应速率,等于化学计量数之比,说明到达平衡,正确;③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,错误;④正反应的速率与逆反应的速率相等,说明到达平衡状态,正确;⑤混合物中各物质的浓度不再变化,反应到达平衡状态,正确。故正确的是②④⑤。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)
步骤1:用碳酸钠溶液洗去铁屑表面的油污。
步骤2:加入稍过量的稀硫酸,保持50~80℃,充分反应后,过滤。
步骤3:将滤液与稍过量的NH4HCO3溶液混合,得到FeCO3的浊液。
步骤4: 、 、 ,得到FeCO3固体。
步骤5:煅烧FeCO3,得到Fe2O3固体。
(1)步骤2中,如何判断反应已经充分? 。
(2)步骤2所得的滤渣中主要含有一种铁的化合物W(Fe3C),经以下处理后,回收利用:W在足量的空气中高温煅烧,生成有磁性的固体X;将X溶于稀硫酸。
①煅烧时1 mol W消耗O2 mol。
②X溶于稀硫酸的离子方程式为 。
(3)步骤3生成FeCO3反应的化学方程式为 。
(4)将步骤4补充完整: 、 、 。
(5)若煅烧时条件控制不当,会使产品中存在杂质FeO。
①若要设计实验检验产品中是否存在FeO,且只能选用两种试剂,这两种试剂是 。
②现煅烧116.0 kg的FeCO3,得到79.2 kg产品,则该产品的纯度为__________。(设产品中只有一种杂质FeO,计算结果保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为短周期内除稀有气体外的元素,它们的原子序数依次增大。四种元素中只有C为金属元素;A和C的最外层电子数相等;B、D属于同主族;C、D两元素原子的质子数之和为A、B两元素原子的质子数之和的3倍。请回答下列问题:
(1)A的元素符号为______,B的原子结构示意图为______。
(2)写出C2B2与A2B反应的离子方程式____ _。
(3)A、B、C、D离子半径由大到小的顺序为 。(用离子符号表示)
(4)用化学方程式证明元素原子的得电子能力B强于D__ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)基态硅原子的电子排布式:_______________。
(2)有一类组成最简单的有机硅化合物叫硅烷。硅烷的组成、结构与相应的烷烃相似。硅烷中硅采取____杂化方式,硅烷的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是_______________。
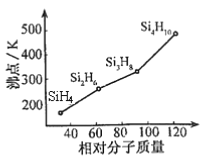
(3)硒和硫同为VIA族元素,与其相邻的元素有砷和溴,则三种元素的电负性由小到大的顺序为_______。 (用元素符号表示)
(4)气态SeO3分子的立体构型为_________,与SeO3互为等电子体的一种离子为____________(填化学式)。
(5)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数比为_________;若该晶体的晶胞棱长为a pm,则该合金密度为______g/cm 3。(列出计算式,不要求计算结果,阿伏伽德罗常数的值为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学课外兴趣小组学生在实验室里制取的乙烯中长混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题
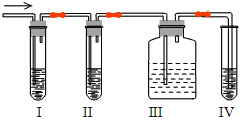
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是I ;Ⅱ ;Ⅲ ;Ⅳ 。依次填为( )
①品红溶液 ②NaOH溶液 ③浓硫酸 ④酸性KMnO4溶液
A.④②①③ B.①②①③ C.①②①④ D.④②①④
(2)能说明SO2气体存在的现象是____________。
(3)使用装置Ⅲ的目的是____________。
(4)确定含有乙烯的现象是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍。试回答:
(1)这四种元素名称分别是:A___________,B___________,C___________,D___________。
(2)这四种元素中在常温常压下的液态或气态氢化物的稳定性由大而小的顺序是_______________。(用化学式表示,下同)
(3)A与B形成的三原子分子的电子式是___________,B与D形成的原子个数比为l∶l的化合物中含有的化学键类型有___________。
(4)写一个能证明A和C的金属性或者非金属性强弱的化学方程式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面列出了几组物质,请将物质的合适组号填写在空格上。
同素异形体 , 同分异构体 。
①金刚石与“足球烯”( C60 ); ② D与T ; ③ 16O、17O和18O ;④ 氧气(O2)与臭氧(O3); ⑤ CH4和CH3CH2CH3 ; ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑦![]() 和
和![]() ; ⑧尿素[CO(NH2)2]和 氰酸铵(NH4CNO)
; ⑧尿素[CO(NH2)2]和 氰酸铵(NH4CNO)
(2)H2O2、KCl、Na2SO4、Na2O2、NH3、O2中只含离子键的是 ,既有极性键又有非极性键的是 。既含离子键又含非极性键的物质的电子式是 ,请用电子式表示只含极性键的物质的形成过程: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,所列字母分别代表一种元素:
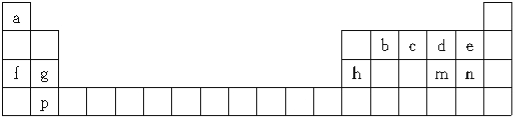
(1)m元素在周期表中的位置是 。
(2)下列有关说法正确的是 (填字母)。
A.b、c、d元素的非金属性逐渐增大 |
B.f、g、h元素的原子半径逐渐减小 |
C.md2与bd2的化学性质类似,都具有氧化性 |
D.e、n的最高价含氧酸的酸性强弱:e>n |
E.a、f分别与d组成的化合物中所含化学键类型完全相同
F.该表中只有4种元素组成的单质具有导电性
(3)a、c、n按原子个数比为4:1:1构成的化合物是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为________。
(2)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为________。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为________,金属晶体K的堆积方式为________。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为______
__________________________________。
(5)100 g上述产气药剂产生的气体通过碱石灰后得到N2 33.6 L(标准状况)。
①用碱石灰除去的物质为________________;
②该产气药剂中NaN3的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com