
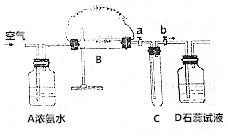
 如图所示,A处通气体,B处加热一段时间后,停止加热,观察现象:
如图所示,A处通气体,B处加热一段时间后,停止加热,观察现象:分析 催化条件下,氨气和氧气反应生成NO和水,反应为放热反应,生成的NO易被氧化生成二氧化氮,为红棕色气体,二氧化氮和水反应生成硝酸,滴加石蕊,溶液变为红色,如氨水浓度过低,可加入具有吸水性的物质,以此解答该题.
解答 解:(1)催化条件下,氨气和氧气反应生成NO和水,反应为放热反应,可观察到铂丝保持红热,反应的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:铂丝保持红热;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)生成的NO易被氧化生成二氧化氮,为红棕色气体,部分二氧化氮和水反应生成硝酸,氨气与硝酸反应生成硝酸铵,可观察到有少量白烟生成,
故答案为:红棕;硝酸铵;
(3)二氧化氮和水反应生成硝酸,滴加石蕊,溶液变为红色,故答案为:红;
(4)如氨水浓度过低,可加入具有吸水性的物质,应加入氢氧化钠或碱石灰,另外两种药品因与氨气反应,不能用作干燥剂,故答案为:③④.
点评 本题综合考查氨气的制备以及性质实验,为高频考点,侧重于学生的分析能力和和实验能力的考查,注意把握实验的原理以及实验的操作方法,难度不大.


科目:高中化学 来源: 题型:选择题
| 元素 | 有关性质及结构信息 |
| X | 所有已知晶体中硬度最大 |
| Y | Y原子的最高价氧化物和气态氢化物能化合成一种盐 |
| Z | 其氢氧化物溶于强碱溶液但不溶于水 |
| W | 其单质常存在于火山喷口处 |
| A. | Y、Z形成的简单离子半径大小关系是Y<Z | |
| B. | H-W键与H-Y键键能较大的是H-W键 | |
| C. | XW2可清洗附着在试管内壁的硫 | |
| D. | Z2W3不能与水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl- | |
| B. | NaHS溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | 通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=10-13mol•L-1的溶液中:NH4+、Mg2+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | Al(OH)3与过量NaOH溶液反应:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | Al(OH)3与过量盐酸反应:Al(OH)3+H+═Al3++3H2O | |
| D. | AlCl3溶液中加入过量NaOH溶液:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.01mol•L-1的醋酸溶液中,pC(H+)=2 | |
| B. | 常温下,向0.01mol•L-1的氨水中加入等体积等浓度的盐酸,混合液的pC(H+)<7 | |
| C. | 100℃时,0.01mol•L-1的NaOH溶液中,pC(OH-)+pC(H+)=14 | |
| D. | 100℃时,CaCO3的Ksp=2.5×10-9,其饱和溶液中pC(Ca2+)+pC(CO32-)=9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ca2+、Cl-、SO42- | B. | Al3+、Na+、SO32-、HCO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
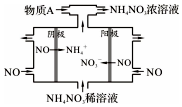 NO2是形成雾霾天气的原因之一.
NO2是形成雾霾天气的原因之一.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液的pH减小 | B. | 溶液中所有离子的浓度减小 | ||
| C. | 氨水的电离程度变大 | D. | 氨水的电离平衡常数Kb不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com