
| 选项 | 目的 | 分离方法 | 原理 |
| A | 除去KCl中的MnO2 | 蒸发结晶 | 溶解度不同 |
| B | 除去碘中的NaCl | 加热、升华 | NaCl的熔点高,碘易升华 |
| C | 分离KNO3和NaCl | 重结晶 | KNO3的溶解度大于NaCl |
| D | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.MnO2不溶于水,KCl溶于水;
B.加热碘易升华,NaCl无变化;
C.二者溶解度受温度影响不同;
D.二者互溶,但沸点不同.
解答 解:A.MnO2不溶于水,KCl溶于水,则溶于水、过滤、蒸发可分离,故A错误;
B.加热碘易升华,NaCl无变化,则加热、升华可分离,故B正确;
C.二者溶解度受温度影响不同,则选择结晶法分离,原理不合理,故C错误;
D.二者互溶,但沸点不同,选择分液法分离,原理不合理,故D错误;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 配合物中中心原子的电荷数和配位数均为6 | |
| B. | Pt4+提供孤对电子 | |
| C. | Cl-和NH3分子均与Pt4+配位 | |
| D. | 配合物中Cl-与Pt4+配位,而NH3分子不配位 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热坩埚中的硫酸铜晶体,失水后须在干燥器中冷却,再称量 | |
| B. | 检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2悬浊液并加热 | |
| C. | 用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 | |
| D. | 做锌铜稀硫酸原电池实验时,反应一段时间后锌片表面还是呈银白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5Cl2+I2+6H2O=10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | |
| C. | MnO2+4HCl=MnCl2+2H2O+Cl2↑ | |
| D. | 2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$ 2NaOH+Cl2↑+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只用蒸馏水无法鉴别一瓶无色液体是苯还是水 | |
| B. | 碘的苯溶液呈紫色,可用蒸馏法将其进一步分离 | |
| C. | 蒸发完成时,用手直接取下蒸发皿放在石棉网上 | |
| D. | 已知汽油是无色液体,不溶于水,密度小于水,分离水和汽油的最合理方法为蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液:NH4+、Mg2+、SO42-、NO3- | |
| B. | 1.0mol/L的NaOH溶液:H+、Cu2+、I-、SO42- | |
| C. | c(H+)=0.001mol/L的溶液:Na+、K+、SiO32-、NO3- | |
| D. | 能使含NH4+的溶液放出NH3的溶液:Na+、Mg2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定没有N2,HCl 和CO中至少有一种 | |
| B. | 一定有N2,HCl 和CO | |
| C. | 一定有N2HCl 和CO中至少有一种 | |
| D. | 一定有N2 和HCl,没有CO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积为11.2 L | B. | 摩尔质量是32g/mol | ||
| C. | 质量为64g | D. | 约含有6.02×1023个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
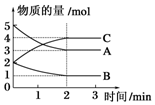 在2L固定容积的密闭容器中,在不同反应时间各物质的物质的量的变化情况如图所示.
在2L固定容积的密闭容器中,在不同反应时间各物质的物质的量的变化情况如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com