
分析 ①制备胶体的原理是利用铁离子水解生成氢氧化铁胶体;
②胶体遇电解质发生聚沉,生成的Fe(OH)3沉淀能与碘化氢发生中和反应.
解答 解:①制备胶体的原理是利用铁离子水解生成氢氧化铁胶体,反应的离子方程式为Fe3++3H2O=Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O=Fe(OH)3(胶体)+3H+;
②加入电解质后,Fe(OH)3胶体发生聚沉,随后沉淀溶解,溶液呈黄色,这是氢氧化铁被HI溶解所致,此反应的离子方程式为:2Fe(OH)3+6H++2I-=I2+2 Fe2++6H2O,故答案为:2Fe(OH)3+6H++2I-=I2+2 Fe2++6H2O.
点评 本题考查胶体的性质和离子方程式的书写,题目难度不大,注意HI既有酸性又有强还原性,I-能使Fe(OH)3胶粒聚沉,H+使其溶解.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
| A. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO | |
| B. | 将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol | |
| C. | 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 | |
| D. | 用惰性电极电解MgCI2溶液:2 Cl-+2H2O=CI2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42- | |
| B. | 通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I- | |
| C. | 加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+ | |
| D. | 加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液一定有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥ | B. | ②⑤ | C. | ①③④ | D. | ②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝溶于氢氧化钠溶液:Al+2OH-+H2O═AlO2-+2H2↑ | |
| B. | 铜片投入少量FeCl3溶液中:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C. | Ca(HCO3)2溶液与足量澄清石灰水混合:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 用铁棒作电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu↓+O2↑+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A(g)+3B(g)?2C(g)反应在密闭容器中进行,若保持容积不变,在温度分别为T1和T2时,达到平衡,B的体积分数与时间的关系如图所示,现象一体积可变的密闭容器中通入等物质的量的A气体和B气体,在恒温条件下发生反应发到平衡状态Ⅰ后,再升高温度,继续反应一段时间后达到平衡状态Ⅱ.下列叙述中正确的是( )
A(g)+3B(g)?2C(g)反应在密闭容器中进行,若保持容积不变,在温度分别为T1和T2时,达到平衡,B的体积分数与时间的关系如图所示,现象一体积可变的密闭容器中通入等物质的量的A气体和B气体,在恒温条件下发生反应发到平衡状态Ⅰ后,再升高温度,继续反应一段时间后达到平衡状态Ⅱ.下列叙述中正确的是( )| A. | T1>T2,该反应生成物的总能量高于反应物的总能量 | |
| B. | 该反应在高温时才能自发进行 | |
| C. | 由平衡状态Ⅰ到平衡状态Ⅱ的过程中,平衡向逆向移动,A的体积分数一直没有变化 | |
| D. | 反映从开始到平衡状态Ⅱ的过程中,平衡常数K和A的转化率都是先增大后减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
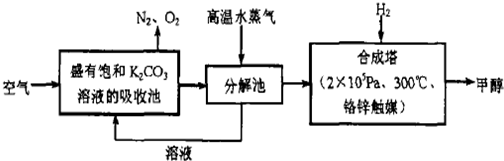
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com