
分析 (1)题给信息可知,Fe2+开始沉淀时,Cu2+已经沉淀完全,而Fe3+沉淀完全时,Cu2+未沉淀,故除去溶液中Fe2+,应先加入氧化剂,将Fe2+氧化为Fe3+沉,再调节溶液pH,注意不能引入杂质离子;
(2)NaClO为强碱弱酸盐,水解呈碱性,则加入NaClO,溶液的pH一定增大,另外NaClO可以酸反应生成HClO而导致溶液pH增大,氧化亚铁离子时会有氢离子参加,也导致溶液pH增大;
(3)使Fe3+转化为Fe(OH)3沉淀,应调节溶液的pH,所加物质能与酸反应,注意不能引入新杂质;
(4)根据关系式:lgc(Cu2+)=8.6-2pH计算溶液pH,再结合pH≥3.7时Fe3+沉淀完全判断.
解答 解:(1)题给信息可知,Fe2+开始沉淀时,Cu2+已经沉淀完全,而Fe3+沉淀完全时,Cu2+未沉淀,故除去溶液中Fe2+,应先加入氧化剂,将Fe2+氧化为Fe3+沉,再调节溶液pH,具体方法为:向溶液中加入足量过氧化氢或氯水,充分反应后,调节pH在3.7~4.4之间,最后过滤,
故答案为:向溶液中加入足量过氧化氢或氯水,充分反应后,调节pH在3.7~4.4之间,最后过滤;
(2)NaClO为强碱弱酸盐,水解呈碱性,则加入NaClO,溶液的pH一定增大,另外NaClO可以酸反应生成HClO而导致溶液pH增大,氧化亚铁离子时会有氢离子参加,也导致溶液pH增大,
故答案为:一定增大;
(3)使Fe3+转化为Fe(OH)3沉淀,应调节溶液的pH,所加物质能与酸反应,注意不能引入新杂质,则则可用CuO 或Cu(OH)2或CuCO3,
故答案为:CuO 或Cu(OH)2或CuCO3;
(4)若溶液中c(Cu2+)为1mol/L,根据关系式:lgc(Cu2+)=8.6-2pH,可知溶液pH=4.3,pH≥3.7时Fe3+沉淀完全,故溶液中Fe3+沉淀完全,
故答案为:4.3;能.
点评 本题考查实验方案设计、物质分离提纯等,注意根据离子开始沉淀与沉淀完全的pH进行分析解答,侧重考查学生对数据的分析与迁移应用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径:R<Y<Z | B. | 简单氢化物的热稳定性:R>Y | ||
| C. | R与Y只能形成一种化合物 | D. | 最高价氧化物的水化物酸性:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
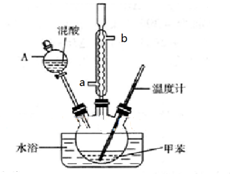
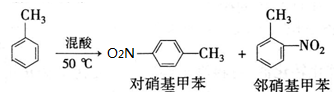
| 密度g•cm-3 | 沸点/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液体烃 |
| 邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液体烃 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )| A. | 2:3 | B. | 1:3 | C. | 3:2 | D. | 2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
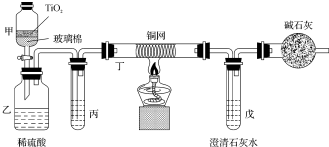
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2的结构式:N≡N | |
| B. | 氯元素的原子结构示意图: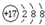 | |
| C. | 中子数为79、质子数为55 的铯(Cs)原子${\;}_{55}^{79}$Cs | |
| D. | 二氧化碳的电子式: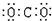 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
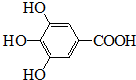 300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水.没食子酸的结构式为:
300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水.没食子酸的结构式为: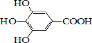 +4NaOH→
+4NaOH→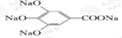 +4H2O.
+4H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com