
【题目】NaCN为剧毒无机物。某兴趣小组查资料得知,实验室里的NaCN溶液可用Na2S2O3溶液进行解毒销毁,他们开展了以下三个实验,请根据要求回答问题:
实验Ⅰ.硫代硫酸钠晶体(Na2S2O3·5H2O)的制备:
已知Na2S2O3·5H2O对热不稳定,超过48℃即开始丢失结晶水。现以Na2CO3和Na2S物质的量之比为2∶1的混合溶液及SO2气体为原料,采用如图装置制备Na2S2O3·5H2O。
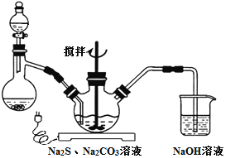
(1)将Na2S和Na2CO3按反应要求的比例一并放入三颈烧瓶中,注入150 mL蒸馏水使其溶解,在蒸馏烧瓶中加入Na2SO3固体,在分液漏斗中注入____________(填以下选择项的字母),并按下图安装好装置,进行反应。
A.稀盐酸 B.浓盐酸 C.70%的硫酸 D.稀硝酸
(2)pH小于7会引起Na2S2O3溶液的变质反应,会出现淡黄色浑浊。反应约半小时,当溶液pH接近或不小于7时,即可停止通气和加热。如果通入SO2过量,发生的化学反应方程式为________________;
实验Ⅱ.产品纯度的检测:
(3)已知:Na2S2O3·5H2O的摩尔质量为248 g/mol;2Na2S2O3+I2=2NaI+Na2S4O6。取晶体样品a g,加水溶解后,滴入几滴淀粉溶液,用0.010 mol/L碘水滴定到终点时,消耗碘水溶液v mL。①滴定终点的现象是 ;②该样品纯度是______________________;
(4)滴定过程中可能造成实验结果偏低的是___________________;
A.锥形瓶未用Na2S2O3溶液润洗
B.锥形瓶中溶液变蓝后立刻停止滴定,进行读数
C.滴定终点时仰视读数
D.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡
实验Ⅲ.有毒废水的处理:
(5)兴趣小组的同学在采取系列防护措施及老师的指导下进行以下实验:
向装有2 mL 0.1 mol/L 的NaCN溶液的试管中滴加2 mL 0.1mol/L 的Na2S2O3溶液,两反应物恰好完全反应,但无明显现象,取反应后的溶液少许滴入盛有10 mL 0.1 mol/L FeCl3溶液的小烧杯,溶液呈现血红色,请写出Na2S2O3解毒的离子反应方程式____________________。
【答案】
(1)C;
(2)Na2S2O3+ SO2+H2O=2 NaHSO3+S↓;
(3)①最后滴入一滴碘水,溶液颜色变成蓝色,且半分钟内部变色;②![]() %;
%;
(4)BD;
(5)CN-+S2O32-=SCN-+SO32-。
【解析】
试题分析:(1)二氧化硫易溶于水,所以不能用稀酸,浓硫酸中氢离子浓度很小,不利于与亚硫酸钠固体反应,所以制备二氧化硫用中等浓度的硫酸;故答案为:C;
(2)Na2S2O3中S的化合价为+2价,pH小于7会引起Na2S2O3溶液的变质反应,会出现淡黄色浑浊。是Na2S2O3发生了歧化反应,生成了亚硫酸钠和硫沉淀,通入SO2过量,与生成的亚硫酸钠反应生成亚硫酸氢钠,反应的化学反应方程式为Na2S2O3+ SO2+H2O=2 NaHSO3+S↓,故答案为:Na2S2O3+ SO2+H2O=2 NaHSO3+S↓;
(3)①滴定终点时,溶液颜色变成蓝色,且半分钟内部变色,故答案为:最后滴入一滴碘水,溶液颜色变成蓝色,且半分钟内部变色;
②vmL0.010mol/L碘水溶液中n(I2)=v×10-3L×0.010mol/L=v×10-5mol,则:
2Na2 S2O3~~~~~~~I2
2 1
n(Na2 S2O3) v×10-5mol
所以n(Na2 S2O3)=2×v×10-5mol=2v×10-5mol,Na2 S2O35H2O晶体的质量为2v×10-5mol×248g/mol=496v×10-5g,则该样品纯度为![]() ×100%=
×100%=![]() %,故答案为:
%,故答案为:![]() %;
%;
(4)A.滴定实验中,锥形瓶不能用Na2S2O3溶液润洗,因此对实验结果无影响,不选;B.锥形瓶中溶液变蓝后立刻停止滴定,进行读数,导致碘水的体积偏小,实验结果偏低,正确;C.滴定终点时仰视读数,使得实验终点读数偏大,溶液体积偏大,实验结果偏大,不选;D.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡,导致实验终点读数偏小,溶液体积偏小,实验结果偏低,正确;故选BD;
(5)根据实验现象,说明反应生成了SCN-,2 mL 0.1 mol/L 的NaCN溶液的试管中滴加2 mL 0.1mol/L 的Na2S2O3溶液,溶质的物质的量之比1:1,结合质量守恒和电荷守恒可知,Na2S2O3解毒的离子反应方程式为CN-+S2O32-=SCN-+SO32-,故答案为:CN-+S2O32-=SCN-+SO32-。


科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、N的原子序数依次增大,其中X的一种同位素原子没有中子,Y的一种核素可做考古学家测文物的年代,Z为地壳中含量最多的非金属元素,相同质量的W的单质在空气中缓慢氧化的产物与其在空气中燃烧产物不同,但转移的电子数相同,N原子为所在周期中原子半径最小的原子(稀有气体除外)。
(1)写出X元素没有中子的原子符号___________;Y与X形成的X元素的质量分数最高的分子的结构式___________;X、Z、N形成的原子个数比1:1:1的分子的电子式___________。
(2)用电子式表示W2Z形成过程___________;
(3)Z、W、N的简单离子半径从大到小的顺序___________(用离子符号表示);
(4)甲由上述元素X、Y元素形成的18电子分子,常温下是气态,可燃烧。
①甲分子中若两个H原子被Br取代,则可生成___________种溴代物;
②若把甲与氧气设计成燃烧电池(KOH溶液为电解质溶液),则负极反应的方程式为___________;放电一段时间后溶液的碱性___________(增强、减弱、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于______________;
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是______________(填“极性”或“非极性”)分子.
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4______________H3PO4; HClO4______________HClO3;
(4)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了______________;
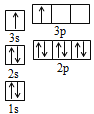
②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A. 乙烯可以作水果的催熟剂
B. 石油分馏属于化学变化
C. 苯燃烧时火焰明亮,伴有浓烟
D. 冶炼金属是将金属从其化合物中还原出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂。
(1)组成氧硫化碳和磷化氢的各原子中,原子半径最大的元素在周期表中的位置是_______________.
(2)下列事实可用于比较C与P两种元素非金属性相对强弱的是_____(填字母)
A.最高正化合价:P>C
B.同温同浓度的两溶液的酸性:H3PO4>H2CO3
C.沸点:PH3>CH4
(3)氧硫化碳水解及部分应用流程如下(部分产物已略去);
![]()
①已知:常温下,反应Ⅱ中每吸收1.7g H2S气体,反应放出热烈4.76kJ,则该反应的热化学方程式为_______________________________。
②已知M溶液中硫元素的主要存在形式为S2O32—,则反应Ⅲ中生成S2O32—的离子方程式为_______________.
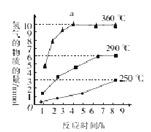
③如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为3mmol)。由图像分析可知,a点时M溶液中除S2O32—外,还有______________(填含硫微粒的离子符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.CO可用于合成甲醇。在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:
CO(g)+2H2(g)![]() CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
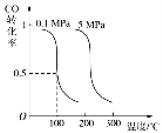
(1)该反应属于 反应(填“吸热”或“放热”)。
(2)100℃时,该反应的平衡常数:K= (用a、b 的代数式表示)。
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率
(填“增大”“不变”或“减小”)
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为 。
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0. 2 mol/ L醋酸溶液,滴定曲线如图所示。
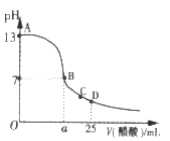
(1)该氢氧化钠溶液浓度为________________。
(2)在B点,a_________12.5 mL(填“<”“>”或“=”)。
(3)在D点,溶液中离子浓度大小关系为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验装置用于制取纯净的无水FeCl3.
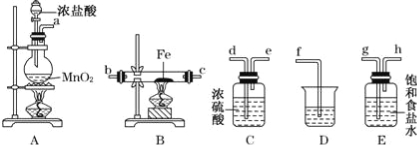
(1)图中盛放浓盐酸的实验仪器的名称为 ,A中发生反应的化学方程式为
(2)各装置的正确连接顺序为:a → → → → → → c → (填字母代号),
(3)装置E的作用是 ,装置C的作用是 。
(4)装置D中所发生反应的离子方程式为 .
(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),则反应中被氧化的HCl的质量为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是
A.SO2、NO、NO2都是大气污染气体,在空气中都能稳定存在
B.Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同,但化学键种类不同
C.SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液呈红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com