

分析 (1)溴水和己烷混合后,下层几乎是无色的,且分液后得到橙色溶液来分析密度、溶解性等;
(2)打开瓶盖瓶口出现白雾,这说明有溴化氢生成,再结合己烷是烷烃,烷烃能和溴发生取代反应生成无色溴代烷和溴化氢来分析;
(3)己烷裂化有气态的烯烃生成,烯烃含有碳碳双键,能使酸性高锰酸钾溶液褪色;
(4)在一定条件下,己烷裂化生成丙烷和丙烯写出方程式.
解答 解:(1)溴水和己烷混合后,下层几乎是无色的,且分液后得到橙色溶液,这说明己烷比水轻,难溶于水,可溶解溴,
故答案为:己烷比水轻,难溶于水,可溶解溴;
(2)由于打开瓶盖瓶口出现白雾,这说明有溴化氢生成,由于己烷是烷烃,烷烃能和溴发生取代反应生成无色溴代烷和溴化氢,因此选AB,
故答案为:AB;
(3)己烷裂化有气态的烯烃生成,烯烃含有碳碳双键,能使酸性高锰酸钾溶液褪色,即试管C中看到的现象是酸性高锰酸钾的紫色褪去,
故答案为:酸性高锰酸钾的紫色褪去;气态烯烃;
(4)在一定条件下,己烷裂化生成丙烷和丙烯,反应的方程式是:CH3(CH2)4CH3$→_{△}^{催化剂}$CH3CH2CH3﹢CH3CH=CH2↑,
故答案为:CH3(CH2)4CH3$→_{△}^{催化剂}$CH3CH2CH3﹢CH3CH=CH2↑.
点评 本题主要考查了物质性质的探究,侧重对学生实验探究能力的培养,有利于培养学生的逻辑推理能力和抽象思维能力,难度中等.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 溴苯中混有溴:加NaOH溶液洗涤、静置、分液 | |
| B. | 除去乙醇中少量乙酸:加入足量生石灰蒸馏 | |
| C. | 乙烯中混有SO2:将其通过盛有酸性KMnO4溶液的洗气瓶,再干燥 | |
| D. | 乙酸乙酯中有乙酸杂质:加入饱和Na2CO3溶液,充分反应后静置分液 |
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关.对下列现象或事实的解释正确的是( )
选项 | 现象或事实 | 解释 | |
A | 用浸有酸性高锰酸钾溶液的硅藻 土作水果保鲜剂 | 酸性高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
|
B | 用氢氟酸蚀刻玻璃 | SiO2是碱性氧化物,能溶于酸 | |
C | 过氧化钠作呼吸面具中的供氧剂 | 过氧化钠是强氧化剂,能氧化二氧化碳 | |
D | Al(OH)3用作塑料的阻燃剂 | Al(OH)3受热熔化放出大量的热 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 恒容充入氮气 | B. | 恒压充入氦气 | C. | 恒容充入氦气 | D. | 恒容降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以海水为原料制得精盐,再电解精盐的水溶液制取钠 | |
| B. | 用海水、石灰乳等为原料,经一系列过程制得氧化镁,用H2还原氧化镁制得镁 | |
| C. | 以铁矿石、焦炭、空气、石灰石等为原料,通过反应产生的CO在高温下还原铁矿石制得铁 | |
| D. | 从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烯和聚乙烯均能发生加成反应 | |
| B. |  和 和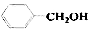 互为同系物 互为同系物 | |
| C. | 用新制氢氧化铜悬浊液能鉴别葡萄糖和乙酸 | |
| D. | 等质量的乙烯和乙醇完全燃烧,消耗氧气的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、HBr、HI的热稳定性依次减弱 | |
| B. | 水加热到很高的温度都难以分解 | |
| C. | CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 | |
| D. | 水结成冰体积膨胀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com