
| A. | 元素电负性:P>F | B. | 第一电离能(I1):P(磷)>Se(硒) | ||
| C. | 离子半径:Cl-<K+ | D. | 熔沸点:MgCl2<AlCl3 |
分析 A.根据同周期元素从左到右电负性逐渐增大,同主族元素电负性从上到下逐渐减小判断;
B.P原子核外最外层电子为半充满状态,难以失去电子;
C.具有相同的核外电子排布的离子,核电荷数越大离子半径越小;
D.AlCl3为共价化合物,熔沸点较低.
解答 解:A.同周期元素从左到右电负性逐渐增大,则有F>N,同主族元素电负性从上到下逐渐减小,则N>P,所以电负性F>P,故A错误;
B.P原子核外最外层电子为半充满状态,难以失去电子,故B正确;
C.具有相同的核外电子排布的离子,核电荷数越大离子半径越小,应为Cl->K+,故C错误;
D.AlCl3为共价化合物,对应的晶体为分子晶体,而氯化镁为离子晶体,故D错误.
故选B.
点评 本题考查元素周期律知识,题目难度不大,本题注意把握元素周期律的递变规律即可解答,注意氯化铝为共价化合物,沸点较低.


科目:高中化学 来源: 题型:选择题
| A. | 只有①②④⑤⑥ | B. | 只有①②③④ | C. | 只有①②④ | D. | 都不行 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 时间 (min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 30 | 120 | 280 | 350 | 370 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
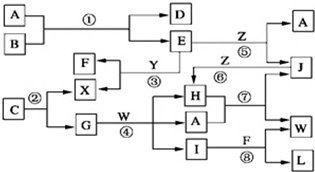
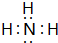
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
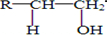 $→_{△}^{浓硫酸}$R-CH=CH2+H2O)
$→_{△}^{浓硫酸}$R-CH=CH2+H2O)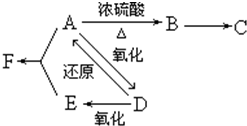
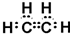 .
.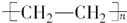
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li是最活泼金属,F是最活泼非金属 | |
| B. | Mg(OH)2碱性比Ca(OH)2强 | |
| C. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 | |
| D. | X2+的核外电子数目为10,则X在第3周期第ⅡA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由苯制硝基苯;由苯制环己烷 | |
| B. | 由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷 | |
| C. | 乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 由苯制溴苯;由乙烷与氯气在光照下的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 非金属元素只能形成共价化合物 | |
| B. | 在NaCl中,除Na+和Cl-的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用 | |
| C. | 任何离子键在形成过程中必定有电子的得与失 | |
| D. | 离子化合物可能含有共价键原子核之间的排斥作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用可再生能源,用超临界二氧化碳替代有机溶剂,注重原子经济性,采用低能耗生产工艺等都是绿色化学的内容 | |
| B. | 13C与14C属于同一种元素,它们互为同位素 | |
| C. | 通过化学变化可以实现235U与238U的相互转化 | |
| D. | 同位素示踪法是研究化学反应历程的手段之一 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com