
【题目】某化学学习小组为了探究镁和二氧化硫的反应产物,进行如下实验。
Ⅰ.设计如图所示装置完成镁和二氧化硫的反应。

(1)宓验室用亚疏酸钠与浓硫酸反应制备SO2,利用的是浓硫酸的___________
a.强氧化性 b.强酸性 c.脱水性 d.腐蚀性
(2)B装置中试剂的名称是_____________;E装置的作用是_________________。
Ⅱ.探究燃烧的反应产物
(3)反应后取C装置中的固体粉末于烧瓶F中,加入稀硫酸,有气体生成
①产生的气体中含有氢气,则可说明固体中含有______________
②将产生的气体通入硫酸铜溶液,出现黑色沉淀,这一现象的原因是______________ (用离子方程式表示)
(4)取出F装置烧瓶中的混合物,经过滤、干燥得到少量固体粉末,为了探究固体粉末的成分,选择下列装置进行实验:
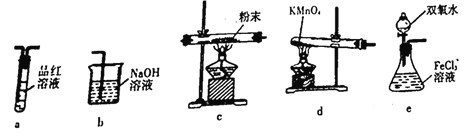
①按气体从左至右,选择所需装置,正确的连接顺序为______________(字母 )
②能证明固体粉末是硫磺的实验现象是_____________________。
(5)经测定,镁在二氧化硫中燃烧生成产物中有硫化镁、硫和氧化镁。如果m(MgO):m(MgS):m(S)=20:7:4,写出镁与SO2在加热条件下反应的化学方程式:________________。
【答案】 b 浓硫酸 吸收尾气中二氧化硫,防止空气中的水和二氧化碳与镁反应 Mg H2S+Cu2+=CuS↓+2H+ dcab 品红溶液褪色 5Mg+2SO2![]() 4MgO+S+MgS
4MgO+S+MgS
【解析】本题主要考查对于探究镁和二氧化硫的反应产物实验的评价。
Ⅰ.(1)宓验室用亚疏酸钠与浓硫酸反应制备SO2,发生复分解反应,利用的是浓硫酸的强酸性,故选b。
(2)B装置用来干燥二氧化硫气体,其中试剂的名称是浓硫酸;E装置的作用是吸收尾气中二氧化硫,防止空气中的水和二氧化碳与镁反应。
Ⅱ.(3)①产生的气体中含有氢气,则可说明固体中含有镁。
②将产生的气体通入硫酸铜溶液,出现黑色沉淀,这一现象的原因是H2S+Cu2+=CuS↓+2H+。
(4) ①按气体从左至右,装置连接顺序为制取氧气,氧气与硫反应,检验二氧化硫,吸收尾气,双氧水不能产生干燥氧气,所以选择d产生氧气,因此,正确的连接顺序为dcab。
②能证明固体粉末是硫磺的实验现象是品红溶液褪色。
(5)经测定,镁在二氧化硫中燃烧生成产物中有硫化镁、硫和氧化镁。如果m(MgO):m(MgS):m(S)=20:7:4,那么,n(MgO):n(MgS):n(S)=4:1:1,因此,镁与SO2在加热条件下反应的化学方程式:5Mg+2SO2 ![]() 4MgO+S+MgS。
4MgO+S+MgS。


科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生反应2HI(g)+Cl2(g)![]() 2HCl(g) + I2(s)。下列事实不能说明该反应到平衡状态的是( )
2HCl(g) + I2(s)。下列事实不能说明该反应到平衡状态的是( )
A. 断裂1 mol Cl-Cl键同时形成1 mol H-Cl键 B. 容器内气体密度不再改变
C. 容器内气体压强不再改变 D. 容器内气体颜色不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】缬氨霉素(valinomycin)是一种脂溶性的抗生素,是由12个分子组成的环状化合物,它的结构简式如图所示,下列有关说法正确的是( )

A. 缬氨霉素是一种蛋白质
B. 缬氨霉素完全水解可得到四种氨基酸
C. 缬氨霉素完全水解后的产物中有三种产物互为同系物
D. 缬氨霉素完全水解,其中一种产物与甘油醛(![]() )互为同分异构体
)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 使甲基橙变红色的溶液:Al3+、Cu2+、I-、S2O32-
B. 常温下,加水冲稀时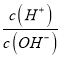 的值明显增大的溶液:CH3COO-、Ba2+、NO3-、Br-
的值明显增大的溶液:CH3COO-、Ba2+、NO3-、Br-
C. 0.1mol·L-1Fe(NO3)2溶液:[Fe(CN)6]3-、Na+、SO42-、Cl-
D. 加入铝粉放出氢气的溶液:K+、Cl-、Mg2+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复)。
阳离子 | Na+、Ba2+、NH |
阴离子 | CH3COO-、OH-、Cl-、SO |
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象。
(1)A是__________,B是____________(填化学式) 。
(2)写出C和D反应的离子方程式________________。
(3)25 ℃时,0.1 mol·L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)=____________________(用含有a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是________________。
(5)在一定体积的0.005 mol·L-1的C溶液中,加入一定体积的0.00125 mol·L-1的盐酸,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. Na2CO3水解的主要产物有CO2
B. 醋酸铵溶液呈中性,是由于醋酸铵不会发生水解
C. 盐的水解可视为中和反应的逆反应
D. 某些盐的水溶液呈中性,这些盐一定是强酸强碱盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25 ℃条件下向10.00 mL 0.1 mol·L-1HCOOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如下图所示(忽略温度变化)。下列说法中不正确的是( )
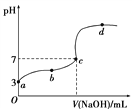
A. a点表示的溶液中c(HCOO-)约为10-3 mol·L-1
B. 用25 mL的酸式滴定管量取HCOOH溶液
C. c点NaOH溶液的体积小于10 mL
D. 在a、c间任一点,溶液中一定都有c(Na+)>c(HCOO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一些硼化合物在工业上有许多用途。以铁硼矿为原料可以制得硼酸及其他硼化合物。回答下列问题:
(1)硼酸(H3BO3)为一元酸,硼酸中B的化合价为__________________。
(2)已知:Ka(H3BO3)=5.8×10-l0,Ka(H2CO3)=4.4×10-7,Ka(HCO3-)=4.7×10-l1,向饱和硼酸溶液中滴加0.1 molL-1Na2CO3溶液,____________(填“能”或“不能”)观察到气泡逸出。写出该反应的化学方程式____________________________________。
(3)以硼酸为原料可制备重要还原剂NaBH4,BH4-的电子式为______________。NaBH4与BF3在50℃~70℃反应生成NaBF4和乙硼烷(B2H6),该反应的化学方程式是___________________________。
(4)硫酸溶解铁硼矿可制得含Fe3+、Fe2+、Al3+杂质的硼酸溶液,提纯过程中加入H2O2的目的是____________________,为除去Fe3+、Al3+ (使其浓度均小于1×10-6 mol·L-1),需至少调节pH=_________(已知: Ksp[Al(OH)3]= 1×10-33,Ksp[Fe(OH)3]=4×10-38)
(5)H3BO3可以通过电解的方法制备。其工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
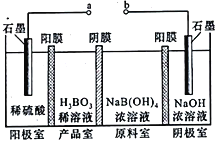
①a接电源的____________ (填“正极”、“ 负极”)
②写出阳极的电极反应式__________________________________。
③原料室中阴、阳离子是如何迁移的?_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是
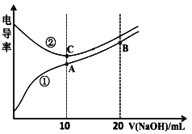
A. 曲线①代表滴定CH3COOH溶液的曲线
B. A、C两点对应溶液均呈中性
C. B点溶液中:c(Na+) > c(OH-) > c(CH3COO-)
D. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com