
(15分)
甲醇是一种可再生能源,具有广泛的开发和应用前景.请回答下列与甲醇有关的问题.
(1)甲醇分子是____分子(填“极性”或“非极性”).
(2)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g) CH3OH(g) △H=-86.6kJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2:,反应达到平衡时,容器内的压强是开始时的3/5.
CH3OH(g) △H=-86.6kJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2:,反应达到平衡时,容器内的压强是开始时的3/5.
①达到平衡时,CO的转化率为 。
②下列选项能判断该反应达到平衡状态的依据的有____ 。
A.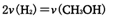 B.CO的消耗速率等于CH3OH的生成速率
B.CO的消耗速率等于CH3OH的生成速率
C.容器内的压强保持不变 D.混合气体的密度保持不变
E.混合气体的颜色保持不变 F.混合气体的平均相对分子质量不随时间而变化
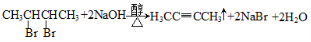 (3)已知在常温常压下:
(3)已知在常温常压下:
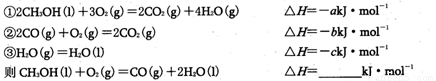
(4)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为____
②若以该电池为电源,用石墨做电极电解200mL含有如下离子的溶液.

电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为 。
(15分)
(1)极性(2分)
(2)60%(2分) CF(2分,全对得2分,只选1个且正确的得1分,选错1个扣1分,扣完为止)
(3)(b-a-4c)/2(3分)
(4)CH3OH-6e-+8OH-=CO32-+6H2O(3分) 3.2g(3分,数值正确、未写单位的扣1分)
【解析】
试题分析:(1) 甲醇分子的正负电荷重心不重合,所以甲醇是极性分子;
(2)①:设消耗CO的物质的量为xmol,则CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
开始时(mol) 1 2 0
消耗(mol) x 2x x
平衡时(mol)1-x 2-2x x
根据题意可得1-x+2-2x+x=3/5(1+2)
解得x=0.6
所以CO的转化率为0.6mol/1mol×100%=60%
②A、未指明正逆反应且比例关系不符合化学计量数之比,错误;B、CO的消耗速率等于CH3OH的生成速率,均是正反应速率,未达平衡也符合,错误;C、恒容条件下,该反应的气体压强开始时一直减小,达平衡时不再变化,正确;D、恒容条件下,气体的总质量不变,所以气体的密度始终不变,错误;E、该反应中的气体均无色,错误;F、气体的总质量不变,物质的量在减小,混合气体的平均相对分子质量在减小,达平衡时,混合气体的平均相对分子质量不再变化,正确,答案选CF。
(3)根据盖斯定律,目标方程式=1/2(①-②)+2×③,所以△H=1/2(b-a)-2c=(b-a-4c)/2;
(4)①燃料电池的负极是燃料发生氧化反应,结合电解质溶液,所以负极的电极反应式为
CH3OH-6e-+8OH-=CO32-+6H2O
②溶液中各离子的物质的量分别为:n(Cu2+)=0.1mol,n(Cl-)=0.4mol,电解开始时,阳极是氯离子放电生成氯气2Cl---2e-=Cl2↑,阴极是Cu2++2e-==Cu,当0.1molCu2+放电完毕后H+放电2H++2e-==H2↑,此时阳极生成0.1mol氯气;随后阴极和阳极产生的氢气和氯气的物质的量相等,只有氯离子放电完毕后,才有可能两极产生的气体体积相等。当氯离子放电完毕,OH-开始放电时两极产生的气体的物质的量分别是阳极:Cl2 0.2mol,阴极:H2 0.1mol;设当生成O2xmol时两极产生的气体相等,则阴极又产生H22xmol,所以0.2+x=0.1+2x,解得x=0.1mol,所以氧气得质量为3.2g;
考点:考查分子极性的判断,化学平衡的计算,盖斯定律的应用, 电化学原理的应用


科目:高中化学 来源:2013-2014重庆市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列与OH—具有相同的质子数和电子数的微粒是( )
A.CH4 B.NH4+ C.Cl— D.NH2—
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市六校高三5月第三次诊断性考试理综化学试卷(解析版) 题型:选择题
用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H=-574 kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ/mol
③H2O(g)=H2O(l) △H=-44kJ/mol。下列说法不正确的是
A.等物质的量的CH4参加反应,反应①②转移的电子数相同
B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-530 kJ/mol
C.0.2 mol CH4还原NO2至N2,且生成H2O(g)放出的热量为164.6 kJ
D.若用4.48 L(标准状况)CH4还原NO2至N2且生成H2O(g),整个过程中转移电子1.60 mol
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市主城七区高三下学期第二次联考理综化学试卷(解析版) 题型:选择题
下列物质的水溶液因发生水解而显酸性的是
A.NH4Cl B.KHSO4 C.NaHCO3 D.H2SO4
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期高三第二次诊断测试理科综合化学试卷(解析版) 题型:选择题
某小分子抗癌药物的分子结构如题图所示,下列说法正确的是

A.1mol该有机物最多可以和5mol NaOH反应
B.该有机物容易发生加成、取代、中和、消去等反应
C.该有机物遇FeCl3溶液不变色,但可使酸性KMnO4溶液褪色
D.1mol该有机物与浓溴水反应,最多消耗3mol Br2
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市万州区高三考前模拟理综化学化学试卷(解析版) 题型:选择题
有A、B、C、D、E五种短周期的主族元素,其原子序数依次增大.B、D在周期表中的相对位置关系如图.下列说法正确的是

A.E元素位于周期表中的第三周期、ⅥA族
B.B的简单阴离子比D的简单阴离子还原性强
C.B与C形成的化合物中一定含有共价键
D.A、B两元素形成的常见化合物的分子构型均为直线型
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高二下学期期末考试化学试卷(解析版) 题型:填空题
(15分)从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:

(1)乙中所含官能团的名称为 ;
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

设计步骤①的目的是 ;指出①的反应类型 ;
反应②的化学方程式为 (注明反应条件)。
(3)欲检验乙中的含氧官能团,选用下列的一种试剂是__________。
A.溴水 B.酸性高锰酸钾溶液 C.溴的CCl4溶液 D.银氨溶液
(4)乙经过氢化、氧化得到丙( )。写出同时符合下列要求的丙的同分异构体结构简式__________________、_________________
)。写出同时符合下列要求的丙的同分异构体结构简式__________________、_________________
①能发生银镜反应;②能与FeCl3溶液发生显色反应;③核磁共振氢谱图上产生4个吸收峰。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
已知有反应:I2(g)+H2(g) 2HI(g)△H<0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
2HI(g)△H<0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
选项 | X | Y |
|
A | 温度 | 容器内混合气体的密度 | |
B | I2的物质的量 | H2的转化率 | |
C | H2的浓度 | 平衡常数K | |
D | 加入Ar的物质的量 | 逆反应速率 |
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:选择题
化学已经渗透到人类生活的各个方面,下列说法不正确的是
A.2011年3月11日,日本发生大地震,并引发核电厂爆炸,核反应属于物理变化
B.“光化学烟雾”、“臭氧空洞”、“硝酸酸雨”的形成都与氮氧化合物有关
C.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放
D.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com