
常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
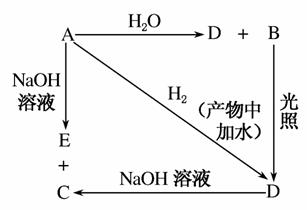
(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A________;B________;C________;
D________;E________。
(2)写出下列反应的化学方程式(请注明条件):
A+H2O_________________________________________。
A+NaOH_______________________________________。
科目:高中化学 来源: 题型:
下列各组离子一定能大量共存的是( )
A.强酸性溶液中:K+、Fe2+、Cl-、NO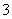
B.强碱溶液中:Na+、K+、[Al(OH)4]-、CO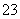
C.强碱性溶液中:NH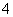 、Al3+、SO
、Al3+、SO 、NO
、NO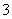
D.含大量Fe3+的溶液中:NH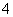 、Na+、Cl-、SCN-
、Na+、Cl-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中,正确的是( )
A.配制5% NaCl溶液时,将已准确称量的NaCl放入烧杯中并加适量的水搅拌溶解
B.配制1 mol·L-1 NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶
C.配制0.1 mol·L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
D.配制1 mol·L-1 Na2CO3溶液500 mL,将Na2CO3放在托盘天平右盘称量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.人们可以利用先进的化学技术和设备制造新的原子
B.人们可以利用催化剂使水变成汽油
C.人们可以利用先进的技术和设备制造新的分子
D.化学科学只能通过实验来探讨物质的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图,下列说法正确的是( )
| X | Y |
| Z | W |
|
| A. | 非金属性:X<Y<Z |
|
| B. | W的原子序数可能是Y的原子序数的2倍 |
|
| C. | 气态氢化物稳定性:Y<W |
|
| D. | Z的化学活泼性一定比X 强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同.
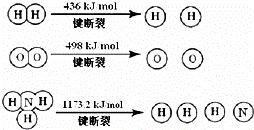
已知:2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol
3H2(g)+N2(g)⇌2NH3(g)△H=﹣92.4kJ/mol
计算断裂1mol N≡N键需要能量 kJ,氮气分子中化学键比氧气分子中的化学键 (填“强”或“弱”),因此氢气与二者反应的条件不同.
(2)固氮是科学家致力研究的重要课题.自然界中存在天然的大气固氮过程:N2(g)+O2(g)=2NO(g)△H=+180.8kJ/mol,工业合成氨则是人工固氮.分析两种固氮反应的平衡常数,下列结论正确的是 .
| 反应 | 大气固氮 | 工业固氮 |
| |||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10﹣31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
A.常温下,大气固氮几乎不可能进行,而工业固氮非常容易进行
B.人类大规模模拟大气固氮是无意义的
C.工业固氮温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大
(3)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:3H2(g)+N2(g)⇌2NH3(g)测得甲容器中H2的转化率为40%.
| N2 | H2 | NH3 | |
| 甲 | 1 | 3 | 0 |
| 乙 | 0.5 | 1.5 | 1 |
| 丙 | 0 | 0 | 4 |
①判断乙容器中反应进行的方向 .(填“正向”或“逆向”)
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为 .
(4)氨气是合成硝酸的原料,写出氨气与氧气反应生成一氧化氮和气态水的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机高分子化合物的部分结构如下:
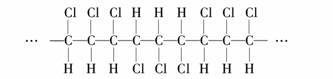
下列说法正确的是(双选)( )
A.聚合物的链节是
B.聚合物的分子式是C3H3Cl3
C.聚合物的单体是CHCl===CHCl
D.若n为聚合度,则其相对分子质量为97n
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com