
【题目】下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是( )
A. 苯中含苯酚杂质:加入溴水,过滤
B. 用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷
C. 乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液
D. 乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用于汽车刹车片的聚合物Y是一种聚酰胺纤维,合成路线如下:
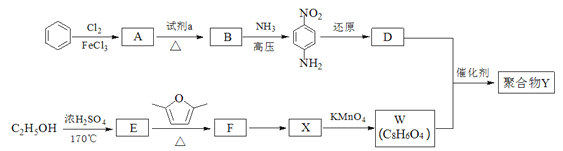
已知:①
②W、D均为芳香化合物,分子中均只含两种不同化学环境的氢原子。
(1)生成A的反应类型是______,试剂a是______,B中所含的官能团名称是_______。
(2)①F的结构简式是______。
②“F→X”的反应中,除X外,另外一种产物是______。
③生成聚合物Y的化学方程式是_______。
(3)Q是W的同系物且相对分子质量比W大14,则Q有_____种,其中核磁共振氢谱有4组峰,且峰面积比为1:2:2:3的为________、__________(写结构简式)。
(4)只以CH2=CH-CH=CH2为有机原料,选用必要的无机试剂合成![]() ,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知 Fe3+在pH=5时沉淀完全)。其中分析错误的是( )
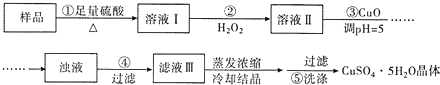
A.步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O
B.步骤②可用氯水、硝酸等强氧化剂代替H2O2
C.步骤③用 CuCO3代替CuO也可调节溶液的pH
D.步骤⑤的操作为:向漏斗中加人少量冷的蒸馏水至浸没晶体,待水自然流下,重复操作2-3次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,HCl被氧化的是( )
A. NaOH+HCl===NaCl+H2O B. Fe+2HCl===FeCl2+H2↑
C. CuO+2HCl===CuCl2+H2O D. MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废液的综合利用有利于减少重金属对水体的污染。某实验小组用以下流程模拟利用一定量工业电镀废液(强酸性,含Cr2O72-、杂质Cu2+等)制备水溶性皮革鞣剂Cr(OH)SO4。回答下列问题:
(已知lg2=0.3,Ksp[ Cr(OH)3]=6.4×10-31, Ksp[ Cu(OH)2]=2×10-20 )
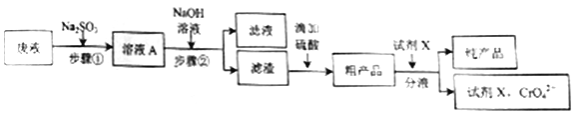
(1)加Na2SO3前先将废液调为弱酸性溶液的原因是__________________,写出废液中加Na2SO3时发生反应的离子方程式_____________。
(2)步骤①须保持温度在30~50℃,可采用的措施是___________________。
(3)步骤②的操作名称是___________。
(4)若在步骤②中,使Cr3+完全沉淀,则溶液的pH范围为______________,
[已知溶液中c(Cu2+)=2×10-4mol·L-1,完全沉淀时c(Cr3+)<10-5 mol·L-1]
(5)粗产品中含有微量CrO42-,工业选择的试剂X应满足的条件是__________。
A.与水互不相溶 B.CrO42-在X中溶解度小
C.Cr(OH)SO4在X中溶解度大 D.Cr(OH)SO4与X不反应
(6)若工业电镀废液含0.1mol Cr2O72-,最终制得产品31.35g,则产率为__________。
(7)酸性条件下,蔗糖还原Na2Cr2O7也可制备Cr(OH)SO4:
Na2Cr2O7+NaHSO4+C12H22O11→Cr(OH)SO4+Na2SO4+H2O+CO2(未配平)
①反应中每生成1molCr(OH)SO4,理论上需要C12H22O11_________mol
②将生成液降温至17℃以下,静置,过滤,在80℃时蒸发滤液,得到标准的工业产品,该产品中混有的主要杂质是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是( )
A. 原子最外层电子数:X>Y>Z
B. 单质沸点:X>Y>Z
C. 离子半径:X2->Y+>Z-
D. 原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯、乙醇、乙酸都是常见的有机物,下列说法正确的是
A. 甲烷中混有乙烯,用酸性高锰酸钾溶液除去
B. 乙醇不能使酸性高锰酸钾溶液褪色
C. 酒越陈越香与酯化反应有关
D. 乙醇与乙酸酯化反应时用稀硫酸作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是( )
A. 原子半径:Y>Z>R>T B. 气态氢化物的稳定性:W<R<T
C. 最高价氧化物对应的水化物的碱性:X>Z D. XR2、WR2两种化合物中R的化合价相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com