
【题目】向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应2A(g) + B(g)![]() 3C(g),各物质浓度随时间变化如图1所示。图2为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3~t4阶段为使用催化剂;图1中t0~t1阶段c(B)未画出。
3C(g),各物质浓度随时间变化如图1所示。图2为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3~t4阶段为使用催化剂;图1中t0~t1阶段c(B)未画出。
图1 图2
图2
(1)若t1=15 min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=________。
(2)t4~t5阶段改变的条件为________,B的起始物质的量为________。各阶段平衡时对应的平衡常数如下表所示:
t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
K1 | K2 | K3 | K4 | K5 |
则K1=____________(计算式),K1、K2、K3、K4、K5之间的关系为____________(用“>”“<”或“=”连接)。
(3)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式:2A(g) + B(g)![]() 3C(g) ΔH,用含有a的代数式表达 ΔH = _________。
3C(g) ΔH,用含有a的代数式表达 ΔH = _________。
(4)在相同条件下,若起始时容器中加入4mol A、2 mol B和1.2 mol C,达到平衡时,体系中 C的百分含量比t1时刻C的百分含量________(填“大于”“小于”“等于”)。
【答案】0.02 molL1min1 减小压强 1mol 0.84 K1 = K2 = K3 = K4<K5 +200a kJmol-1 等于
【解析】
(1)15min内,以C浓度变化表示的反应速率为v(C)=![]() =0.02 mol/(Lmin);
=0.02 mol/(Lmin);
(2)t3~t4和t4~t5这两段平衡是不移动的,则只能是压强和催化剂影响的,因此应该推断该反应为等体积变化的反应,t3~t4的平衡比原平衡的速率要快,而t4~t5的速率又变慢,则前者应是加催化剂,因为条件只能用一次,t4~t5段为减小压强;
反应物的浓度降低,生成物的浓度增大,结合图一可知,A为反应物,C为生成物,A的变化为0.2mol/L,C的变化量为0.3mol/L.又由于该反应为等体积变化的反应,所以B为反应物,根据化学反应的速率之比等于化学方程式的计量系数比,该反应的方程式为2A(g)+B(g)![]() 3C(g),所以,△c(B)=
3C(g),所以,△c(B)=![]() △n(A)=
△n(A)=![]() ×0.2mol/L=0.1mol/L,起始2molA所对应的浓度为1mol/L,则体积应是
×0.2mol/L=0.1mol/L,起始2molA所对应的浓度为1mol/L,则体积应是![]() =2L,故B的起始物质的量为n(B)=(0.1mol/L+0.4mol/L)×2L=1.0mol;
=2L,故B的起始物质的量为n(B)=(0.1mol/L+0.4mol/L)×2L=1.0mol;
t1-t2段,处于平衡状态,c(A)平衡=0.8mol/L,c(B)平衡=0.4mol/L,c(C)平衡=0.6mol/L,
K1= =
=![]() =0.84,
=0.84,
t2-t3段,为改变浓度,平衡移动,平衡常数不变,K2=0.84,
t3-t4段,使用催化剂,加快反应,平衡常数不变,K3=0.84,
t4-t5段,为降低压强,反应速率降低,平衡不移动,平衡常数不变,K4=0.84,
t5-t6段,为升高温度,平衡向正反应方向移动,平衡常数增大,
故 K1=K2=K3=K4<K5;
(3)根据方程式计算,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,则反应2molA时,交换热量200akJ,而由图象可知,t5~t6阶段应为升高温度,正反应速率大于逆反应速率,平衡向正反应方向移动,则正反应为吸热反应,所以热化学方程式为2A(g)+B(g)![]() 3C(g)△H=+200a kJ/mol;
3C(g)△H=+200a kJ/mol;
(4)在相同条件下,若起始时容器中加入4mol A、2 mol B和1.2 mol C,各物质的量为原来的二倍,为等效平衡,达到平衡时,体系中 C的百分含量比t1时刻C的百分含量相等。


科目:高中化学 来源: 题型:
【题目】为了证明铜与稀硝酸反应产生NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
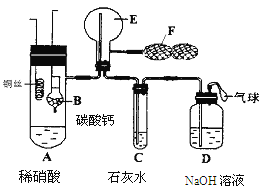
(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为 。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为 。
(3)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是 。
(4)一段时间后,C中白色沉淀溶解,其原因是________________________ __。
(5)装置D的作用是_________ ___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年,中国首次应用六炔基苯在铜片表面合成了石墨炔薄膜(其合成示意图如右图所示),其特殊的电子结构将有望广泛应用于电子材料领域。下列说法不正确的是( )
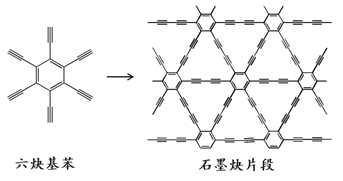
A.六炔基苯的化学式为C18H6
B.六炔基苯和石墨炔都具有平面型结构
C.六炔基苯和石墨炔都可发生加成反应
D.六炔基苯合成石墨炔属于加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2A(g)![]() 2Y(g) + E(g)ΔH>0达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
2Y(g) + E(g)ΔH>0达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
A.加压B.减压C.减小E的浓度D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。CaO2和Na2O2在结构和性质上有很多相似的地方。请完成下列问题:
(1)CaO2属于____(填“离子化合物”或“共价化合物”),其阴、阳离子个数比为______。
(2)CaO2与水反应的化学方程式为______,生成1mol单质气体,转移的电子数为__________。(用NA代表阿伏加德罗常数)
(3)CaO2与二氧化碳反应的化学方程式为_________,该反应属于____________。
A.置换反应 B.氧化还原反应 C.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】公元前一世纪,我国已使用天然气,天然气的主要成分为甲烷。下列关于甲烷的叙述中,错误的是
A. 通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B. 甲烷化学性质比较稳定,不能被任何氧化剂氧化
C. 甲烷跟氧气反应无论生成CH3Cl、CH2Cl、CHCl3还是CCl4,都属于取代反应
D. 甲烷的四种取代物都难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中正确的是

A.1molNH4+所含的质子总数为10NA(设NA为阿伏加德罗常数的值)
B.该方法每处理1molNH4+,需要0.5molNO2-
C.过程IV中,NO2-发生氧化反应
D.N2H2中含有σ键和π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1mol/LNH4Cl溶液中加入足量的镁条,该体系pH随时间变化的曲线如图所示。实验观察到b点开始溶液中有白色沉淀生成,已知Ksp[Mg(OH)2]=1.8×1011。下列说法错误的是

A.常温下,NH4Cl的水解平衡常数数量级为1010
B.体系中,水的电离程度大小关系为![]()
C.![]() 点时,溶液中c(Mg2+)=0.18mol/L
点时,溶液中c(Mg2+)=0.18mol/L
D.a点溶液中,c(NH4+)+c(H+)<c(Cl)+c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处于平衡状态的反应2H2S(g)![]() 2H2(g)+S2(g) ΔH>0,合理的说法是( )
2H2(g)+S2(g) ΔH>0,合理的说法是( )
A. 加入催化剂,反应途径将发生改变,ΔH也将随之改变
B. 升高温度,正逆反应速率都增大,H2S分解率也增大
C. 增大压强,平衡向逆反应方向移动,将引起体系温度降低
D. 若体系恒容,注入一些H2后达新平衡,H2浓度将减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com