
| A. | c1:c2=1:3 | B. | 平衡时,Y与Z的生成速率之比为3:2 | ||
| C. | X、Y的转化率不相等 | D. | c1的取值范围0<c1<0.14 molL-1 |
分析 化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,据此判断分析.
解答 解:若反应向正反应进行到达平衡,X、Y的浓度最大,Z的浓度最小,假定完全反应,则:
根据方程式 X(气)+3Y(气)?2Z(气),
开始(mol/L):c1 c2 c3
变化(mol/L):0.04 0.12 0.08
平衡(mol/L):0.1 0.3 0.08
c1=0,14 c2=0.42 c3=0
若反应逆正反应进行到达平衡,X、Y的浓度最小,Z的浓度最大,假定完全反应,则:
根据方程式 X(气)+3Y(气)?2Z(气),
开始(mol/L):c1 c2 c3
变化(mol/L):0.1 0.3 0.2
平衡(mol/L):0.1 0.3 0.08
c1=0 c2=0 c3=0.28
由于为可逆反应,物质不能完全转化所以起始时浓度范围为0<c(X)<0.14,0<c(Y)<0.42,0<c(Z)<0.28,
A、X 和Y平衡浓度为1:3,变化的量为1;3,所以起始量为1:3,c1:c2=1:3,故A正确;
B、平衡时,Y和Z的生成速率之比为化学方程式系数之比为3:2,故B正确;
C、X、Y的变化量之比和起始量之比相同,所以转化率相同,故C错误;
D、依据上述计算,c1的取值范围为0<c1<0.14mol•L-1,故D正确;
故选C.
点评 本题考查了化学平衡的建立可以逆向进行,也可以正向进行,依据极值法进行转化计算分析判断是本题的关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(l)△H<0 | B. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H<0 | ||
| C. | HCl(aq)+NaOH (aq)=NaCl(aq)+H2O(l)△H<0 | D. | 4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe (OH)3(s)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
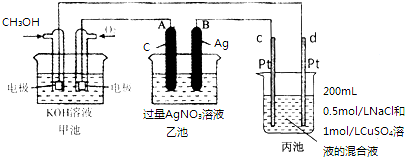
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、NO${\;}_{3}^{-}$、K+、SO${\;}_{4}^{2-}$ | B. | Cu2+、Ba2+、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$ | ||
| C. | OH-、Cl-、NH${\;}_{4}^{+}$、Na+ | D. | Mg2+、Na+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 选用试剂 | 操作方法 |
| A | CO2(CO) | 过量O2 | 点燃 |
| B | CaO(CaCO3) | 足量蒸馏水 | 过滤、蒸发 |
| C | NaCl溶液(MgSO4溶液) | 适量BaCl2溶液 | 过滤 |
| D | FeCl2溶液(CuCl2溶液) | 足量铁粉 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com