
| A. | 除④外都对 | B. | 除⑤外都对 | C. | ④⑤不对 | D. | 全都正确 |
分析 ①根据稀HNO3可与银反应,所以可用稀HNO3清洗做过银镜反应的试管进行解答;
②根据碘易溶于酒精进行解答;
③根据高锰酸钾分解生成难溶于水的二氧化锰,浓盐酸可以和二氧化锰反应进行解答;
④根据长期盛放FeCl3溶液的试剂瓶中含有氢氧化铁,氢氧化铁能与盐酸反应进行解答;
⑤根据氢氧化钠溶液能硫反应生成硫化钠、亚硫酸钠和水进行解答.
解答 解:①稀硝酸具有强氧化性,银具有还原性,银和硝酸发生反应,3Ag+4HNO3═3AgNO3+NO↑+2H2O,生成易溶于水的硝酸银,所以可用稀硝酸洗涤作过银镜反应的试管,除去附在试管上的银,故①正确;
②因碘易溶于酒精,所以可用酒精清洗做过碘升华的烧杯,故②正确;
③高锰酸钾分解生成难溶于水的二氧化锰,浓盐酸可以和二氧化锰反应生成氯化锰、氯气和水,所以可用浓盐酸清洗做过高锰酸钾分解实验的试管,故③正确;
④因长期盛放FeCl3溶液的试剂瓶中含有氢氧化铁,氢氧化铁能与盐酸反应,所以用盐酸清洗长期盛放FeCl3溶液的试剂瓶,故④正确;
⑤氢氧化钠溶液能硫反应生成硫化钠、亚硫酸钠和水,所以可用氢氧化钠溶液清洗沾有硫磺的试管,故⑤正确.
故选D.
点评 本题考查仪器的洗涤,物质的性质决定了物质的用途,熟练掌握物质的性质是解题的关键,难度不大.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 酸性 H2SO4>H3PO4 | B. | 热稳定性 H2S>H2O | ||
| C. | 碱性 NaOH>Mg(OH)2 | D. | 氧化性F2>O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D | |
| A | - | - | ↑ | |
| B | - | ↓ | ↓ | |
| C | - | ↓ | - | |
| D | ↑ | ↓ | - |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
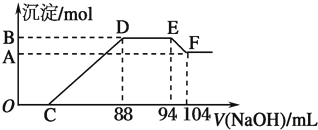
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 目的 | A.实验室制取并收集O2 | B.检验装置气密性 | C.制取蒸馏水 | D.分离水和四氯化碳 |
| 装置或操作 | 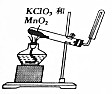 | 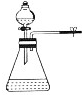 | 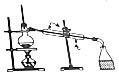 | 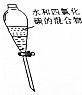 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡正向移动 | B. | 平衡逆向移动 | ||
| C. | 正逆反应速率都增大 | D. | NH3的质量分数增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl中含有35Cl | |
| B. | 生成物Cl2的平均相对分子质量为73.3 | |
| C. | 1molK35ClO3参加反应,失去电子数为5NA | |
| D. | 氧化剂和还原剂的物质的量之比1:6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com