
| A. | 聚乙炔 | B. | 苯乙烯 | C. | 聚氯乙烯 | D. | 聚1,3-丁二烯 |
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:选择题
| A. | 足量CO2与NaOH溶液反应:CO2+2OH-=CO32-+H2O | |
| B. | NaHCO3溶液中加入过量Ba(OH)2溶液:2HCO3-+2OH-+Ba2+=BaCO3↓+CO32-+2H2O | |
| C. | 氯化铝溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Na+、OH-、SO42- | B. | NH4+、Mg2+、NO3-、Cl- | ||
| C. | Ba2+、OH-、Cl-、SO42- | D. | Fe2+、H+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 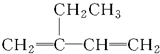 2-乙基-1,3-丁二烯 2-乙基-1,3-丁二烯 | B. | CH3CH2CH2CH2OH 丁醇 | ||
| C. |  甲苯 甲苯 | D. | HOCH2CH2CH2OH 1,3-二丙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 属于正四面体的空间结构 | B. | 分子中的碳原子是饱和的 | ||
| C. | 没有同分异构体 | D. | 是甲烷的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(g)+O2(g)=SO2(g);△H=-Q kJ/mol.Q的值小于297.23 kJ/mol | |
| B. | S(g)+O2(g)=SO2(g);△H=-Q kJ/mol.Q的值大于297.23 kJ/mol | |
| C. | 1mol SO2的键能总和等于1molS和1molO2的键能和 | |
| D. | 1mol SO2的键能总和小于1molS和1molO2的键能和 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com