
 ��
��
���� ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ���Ȼ���д��ڶ���A�Ļ������AΪ��Ԫ�أ�Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬����������6�����ӣ���BΪ̼Ԫ�أ�D�Ļ�̬ԭ�ӵ������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ�Dԭ����Χ�����Ų�Ϊ3d104s1����DΪͭԪ�أ����ԭ��������֪��Cֻ�ܴ��ڵ������ڣ�B��C���γ����������ͷ��ӣ���BΪ��Ԫ�أ�
��1������Ԫ���е縺��������Cl�����̬ԭ�ӵļ۵����Ų�ʽΪ3s23p5��
��2��C2H2�ĽṹʽΪH-C��C-H������Ϊ�Ҽ�����������1���Ҽ���2���м���
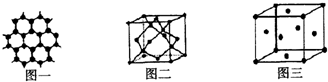
��3��ͼһΪƽ��ṹ�������״�ṹ��̼̼������Ϊ120�㣬ÿ��̼ԭ�Ӷ������3��̼ԭ�ӣ�̼ԭ�Ӳ�ȡsp2�ӻ���
���㾧����̼ԭ��������뾧��������������ռ�������=$\frac{������ԭ�������}{�������}$��100%��������ÿ��Cԭ������Χ4��Cԭ���γ���������ṹ��������������ԭ���뾧������ԭ�������ھ�����Խ����ϣ���Ϊ��Խ��߳��ȵ�$\frac{1}{4}$����
��4������ͭ��Һ�м��백ˮ�����������ͭ��ɫ�����������μӰ�ˮ�������ܽ⣬�õ��İ���ͭ�����ӣ���ҺΪ����ɫ������Һ��
��5���ɾ����ṹʾ��ͼ��֪������Ķѻ�ģ��Ϊ���������ܶѻ������þ�̯�����㾧����ԭ����Ŀ���ټ��㾧�����������������m=��V���㰢��٤��������
��� �⣺ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ���Ȼ���д��ڶ���A�Ļ������AΪ��Ԫ�أ�Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬����������6�����ӣ���BΪ̼Ԫ�أ�D�Ļ�̬ԭ�ӵ������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ�Dԭ����Χ�����Ų�Ϊ3d104s1����DΪͭԪ�أ����ԭ��������֪��Cֻ�ܴ��ڵ������ڣ�B��C���γ����������ͷ��ӣ���BΪ��Ԫ�أ�
��1������Ԫ���е縺��������Cl�����̬ԭ�ӵļ۵����Ų�ʽΪ3s23p5����̬ԭ�ӵļ۵����Ų�ͼΪ ��
��
�ʴ�Ϊ�� ��
��
��2��C2H2�ĽṹʽΪH-C��C-H������Ϊ�Ҽ�����������1���Ҽ���2���м������еĦҼ����м���Ŀ֮��Ϊ3��2��
�ʴ�Ϊ��3��2��
��3��ͼһΪƽ��ṹ�������״�ṹ��̼̼������Ϊ120�㣬ÿ��̼ԭ�Ӷ������3��̼ԭ�ӣ�̼ԭ�Ӳ�ȡsp2�ӻ���
������ÿ��Cԭ������Χ4��Cԭ���γ���������ṹ��������������ԭ���뾧������ԭ�������ھ�����Խ����ϣ���Ϊ��Խ��߳��ȵ�$\frac{1}{4}$����̼ԭ�Ӱ뾶Ϊr�����ⳤΪ8r���ʾ����ⳤΪ$\frac{8\sqrt{3}r}{3}$r��������Cԭ����Ŀ=4+6��$\frac{1}{2}$+8��$\frac{1}{8}$=8������̼ԭ�������=8��$\frac{4}{3}$��r3���ʾ����ռ�������=8��$\frac{4}{3}$��r3�£�$\frac{8\sqrt{3}r}{3}$��3=34%��
�ʴ�Ϊ��sp2��34%��
��4������ͭ��Һ�м��백ˮ�����������ͭ��ɫ�����������μӰ�ˮ�������ܽ⣬�õ��İ���ͭ�����ӣ���ҺΪ����ɫ������Һ����ɫ�����ܽ����ӷ���ʽΪ��Cu��OH��2+4NH3�T[Cu��NH3��4]2++2OH-��
�ʴ�Ϊ��Cu��OH��2+4NH3�T[Cu��NH3��4]2++2OH-��
��5���ɾ����ṹʾ��ͼ��֪������Ķѻ�ģ��Ϊ���������ܶѻ���������ԭ����ĿΪ6��$\frac{1}{2}$+8��$\frac{1}{8}$=4����������Ϊ4��$\frac{Mg/mol}{{N}_{A}}$���������Ϊ��a cm��3����4��$\frac{Mg/mol}{{N}_{A}}$=��g/cm3����a cm��3����NA=$\frac{4M}{��{a}^{3}}$mol-1��
�ʴ�Ϊ��4�����������ܶѻ���$\frac{4M}{��{a}^{3}}$��
���� �����Ƕ����ʽṹ�Ŀ��飬��Ŀ�ۺ��Խϴ��漰Ԫ���ƶϡ���������Ų�������ṹ�����ȣ��Ƕ�ѧ���ۺ������Ŀ��飬��3���о����ռ������ʼ������ѵ㡢�״��㣬��Ҫѧ���߱�һ���Ŀռ���������ѧ����������ѧϰ��ע����ػ����Ļ��ۣ��ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ķ�Ӧ | B�� | �Ȼ�茶�����Ba��OH��2•8H2O�ķ�Ӧ | ||
| C�� | ����صķֽⷴӦ | D�� | �����ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
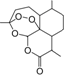 �ҹ�Ů��ѧ�������ϵ����ֳ��ԡ�ʫ��•С�š���������¹����ʳҰ֮����мα����������ѡ������������Ϳ�űҩ---�����أ��ṹ��ͼ����˫�������صĹ��ף��ٻ�2015��ŵ�������������й������ص�����������ǣ�������
�ҹ�Ů��ѧ�������ϵ����ֳ��ԡ�ʫ��•С�š���������¹����ʳҰ֮����мα����������ѡ������������Ϳ�űҩ---�����أ��ṹ��ͼ����˫�������صĹ��ף��ٻ�2015��ŵ�������������й������ص�����������ǣ�������| A�� | ����ʽΪC15H20O5 | B�� | ������C2H5OC2H5 | ||
| C�� | ���������Ѽ������� | D�� | ����NaOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
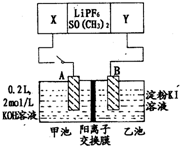 ��֪����﮵�ص��ܷ�ӦʽΪ��2Li+FeS�TFe+Li2S[LiPF6��SO�� CH3��2Ϊ�����]���øõ��Ϊ��Դ������ͼ�ĵ��ʵ�飬���һ��ʱ���ü׳ز�����״����H2 4.48L�������й���������ȷ���ǣ�������
��֪����﮵�ص��ܷ�ӦʽΪ��2Li+FeS�TFe+Li2S[LiPF6��SO�� CH3��2Ϊ�����]���øõ��Ϊ��Դ������ͼ�ĵ��ʵ�飬���һ��ʱ���ü׳ز�����״����H2 4.48L�������й���������ȷ���ǣ�������| A�� | �Ӹ�Ĥ��ͨ����������ĿΪ0.4 NA | |
| B�� | ������������仯���Բ��ƣ������׳�����ҺŨ��Ϊ4 mol/L | |
| C�� | A�缫Ϊ���� | |
| D�� | ��Դ������ӦʽΪ��FeS+2Li++2e-�TFe+Li2S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ú���ʱ�û������ | |
| B�� | ʵ������ͨ������Ʊ����� | |
| C�� | ��ˮ����Ũ��������ϡ���� | |
| D�� | �õ�ȼ�Ļ����Һ������ƿ�ڼ����Ƿ�©�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ˡ��ᾧ�����ա���ȡ����Һ������ȶ��dz��õķ����л������ķ��� | |
| B�� | ϴ�ӽ�ͷ�ι�ʱ��ֻҪ��ˮ��ͷ����ˮ�У���ͷ���ϣ���ͷ���²��ϼ�ѹ��ͷ���� | |
| C�� | ͨ�����ò������ݵĿ��������Ƚϲ�ͬ������Na2S2O3��Һ��ϡ����ķ�Ӧ���� | |
| D�� | �����������Ȼ�������ʱ�������������ƾ������ѵĻ�������ⶾ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�22gCO2��������������������0.5NA | |
| B�� | 1LCO2��1LCO������������ͬ | |
| C�� | ��������O2��O3��������ԭ����һ����� | |
| D�� | 1mol•L-1��NaOH��Һ��Na+��ĿΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com