
| A. | 在家用燃煤中适量的生石灰能有效减少二氧化硫的排放量 | |
| B. | 利用清洁能源如太阳能、潮汐能、风能来发电 | |
| C. | 大量排放 SO2或 CO2 都会导致酸雨的形成 | |
| D. | 采用纳米二氧化钛光触媒技术,将汽车尾气中的 NO 和 CO 转化为无害气体 |
分析 A.二氧化硫与CaO反应,可减少二氧化硫的排放;
B.太阳能、潮汐能、风能为新能源,可减少化石能源的使用;
C.SO2会导致酸雨的形成,溶解CO2的雨水为正常雨水;
D.NO 和 CO 在催化剂作用下反应生成氮气和二氧化碳.
解答 解:A.二氧化硫与CaO反应,可减少二氧化硫的排放,则燃煤中适量的生石灰能有效减少二氧化硫的排放量,故A正确;
B.太阳能、潮汐能、风能为新能源,可减少化石能源的使用,则利用清洁能源如太阳能、潮汐能、风能来发电,故B正确;
C.溶解CO2的雨水为正常雨水,不含导致酸雨发生,故C错误;
D.NO 和 CO 在催化剂作用下反应生成氮气和二氧化碳,则采用纳米二氧化钛光触媒技术,将汽车尾气中的 NO 和 CO 转化为无害气体,故D正确;
故选C.
点评 本题考查三废处理及环境保护,为高频考点,把握常见的环境污染物、化学与环境的联系为解答的关键,侧重分析与应用能力的考查,注意酸雨的成因,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 将硫的酒精溶液滴入一定量的热水中得微蓝色透明液体,用激光笔照射微蓝色透明液体,有光亮的通路 | 微蓝色透明液体为胶体 |
| B | 室温下,向10mL 0.2mol•L-1 AgNO3溶液中滴入2滴0.1 mol•L-1 NaCl溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1NaI溶液,生成黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向某溶液中加入BaCl2溶液,无明显现象,再加稀盐酸,有无色且能使澄清石灰水变浑浊的气体产生 | 溶液中一定含HCO3- |
| D | 取少量CH3CH2Br与NaOH溶液共热,冷却后滴加AgNO3溶液,无淡黄色沉淀出现 | CH3CH2Br没有水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
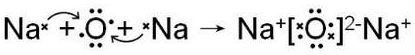 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
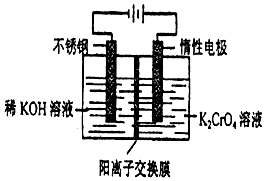 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )| A. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| B. | 在阴极室,通电后KOH溶液不断变浓,并产生气体H2 | |
| C. | CrO42-通过离子交换膜从阳极区域迁移到阴极区域 | |
| D. | 电解一段时间后测定阳极液中K和Cr的物质的量之比为d,则导线中转移电子的物质的量为(2-d)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
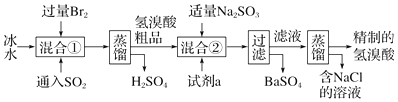
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Na2CO3溶液用水稀释后,pH变大,Kw不变 | |
| B. | 向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变 | |
| C. | pH=4.75浓度均为0.1mol/L的CH3COOH、CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)<c(H+)+c(CH3COOH) | |
| D. | 分别用pH=2和pH=3的CH3COOH溶液中和等物质的量的NaOH,消耗CH3COOH溶液的体积分别为Va和Vb,则10Va>Vb |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验H的 | 实验方案 |
| A | 证明Mg(OH)2沉淀可以转化为 Fe(OH)3 | 向2mL1mol/LNaOH溶液中先加入3滴1mol/LMgCl2溶液,再加入3滴1mol/LFeCl3溶液 |
| B | 比较氯和碳的非属性强弱 | 将盐酸滴入碳酸氢钠溶液中 |
| C | 验证电解饱和食盐水阳极有氯气生成 | 以铁为电极电解饱和食盐水,并将阳极生成的气体通入淀粉-KI溶液 |
| D | 比较铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 向1mL 1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀 | 说明Y中不含醛基 |
| C | 取a g铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为V L(已转化为标准状况下) | 测定铝箔中氧化铝的含量 |
| D | 比较不同反应的反应热数据大小 | 从而判断反应速率的大小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管用待装液润洗 | B. | 锥形瓶振荡时有少量液体溅出 | ||
| C. | 滴定结束后滴定管末端出现气泡 | D. | 锥形瓶用待测液润洗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com