
| A. | 煤的干馏和石油的分馏都属于化学变化 | |
| B. | 石油裂化获得的产品是混合物 | |
| C. | 石油主要含C、H、O三种元素 | |
| D. | 煤焦油经过分馏可得到苯、甲苯等,说明煤中含有苯和甲苯 |
分析 A.煤的干馏、石油的裂化都是化学变化,石油的分馏是物理变化;
B.石油裂化的主要目的是提高轻质液体燃料(汽油,煤油,柴油等)的产量;
C.石油主要是各种烷烃、环烷烃、芳香烃的混合物;
D.煤中不含有苯和甲苯.
解答 解:A.煤的干馏是指将煤隔绝空气加强热使之分解的过程,属于化学变化,石油的分馏是根据物质的沸点不同进行分离的,属于物理变化,故A错误;
B.石油裂化的主要目的是为了提高轻质液体燃料(汽油,煤油,柴油等)的产量,特别是提高汽油的产量,获得的产品是混合物,故B正确;
C.烃为碳氢化合物,石油主要是烃的混合物,主要含C、H两种元素,故C错误;
D.煤中不含苯和甲苯,煤干馏后从煤焦油中能分离出来苯和甲苯,故D错误;
故选B.
点评 本题考查煤、石油综合的利用,掌握煤的干馏、石油的分馏、石油裂化等知识是解答关键,题目较简单.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题

| A. | 某实验需要配制460mL1.0mol/L的稀硫酸,应取该硫酸25.0mL | |
| B. | 足量铜和含2mol溶质的该硫酸在加热条件下反应,标准状况下生成气体的体积约为22.4L | |
| C. | 该硫酸与等质量的水混合所得溶液溶质的物质的量浓度小于9.2mol/L | |
| D. | 该硫酸与等体积的水混合所得溶液的溶质质量分数小于49% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 | |
| B. | 称量时称量物放在称量纸上或玻璃器皿中,置于托盘天平右盘,砝码放在托盘天平的左盘中 | |
| C. | 汽油和水的混合物可用分液的方法分离 | |
| D. | 过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3俗名小苏打 | |
| B. | 在水中的溶解度:Na2CO3>NaHCO3 | |
| C. | 与同浓度的硫酸反应放出气泡的速率:NaHCO3<Na2CO3 | |
| D. | 热稳定性:NaHCO3<Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
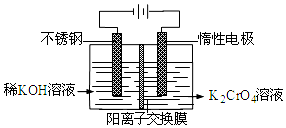
| A. | 在阴极式,发生的电极反应为:2H2O+2e-═2OH-+H2↑ | |
| B. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| C. | 该制备过程总反应的化学方程式为:4K2CrO4+4H2O$\frac{\underline{\;电解\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+O2↑ | |
| D. | 铬原子的价电子排布式为3d44S2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将质量分数为98%的浓硫酸稀释成质量分数为20%的稀硫酸要用容量瓶配制 | |
| B. | 配制100mL1mol/L的氢氧化钠溶液,称量固体质量为4.0g | |
| C. | 容量瓶在定容时,若视线仰视,会使得配制出的溶液物质的量浓度偏小 | |
| D. | 容量瓶洗涤时,若瓶底上有少量蒸馏水,可不必烘干直接使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两次平衡时,C(g)的浓度相等 | |
| B. | 平衡时,单位时间内n(B)生成:n(C)消耗=1:1 | |
| C. | 若再向平衡体系中加入少量A,平衡不移动 | |
| D. | 若开始时向容器中加入1 mol B和1 mol C,则达到平衡时吸收QkJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
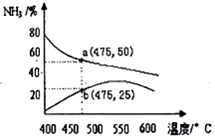 氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用.
氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四个碳原子不可能在一条直线上 | B. | 所有原子在同一平面内 | ||
| C. | 在同一直线上的原子最多为4个 | D. | 在同一直线上的原子最多为6个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com