
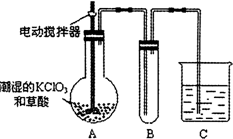
 煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题:
煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题: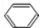 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O;
+H2O;
 .
. 分析 (1)煤的干馏属于化学变化;
(2)防止溶液倒吸;
(3)水层有溶解的氨气,氨水显碱性;苯与浓硝酸、浓硫酸在加热条件下发生取代反应生成硝基苯;
(4)气体A与反应生成B,B可以连续氧化得到D,可知A为CH2=CH2、B为CH3CH2OH、C为CH3CHO、B为CH3COOH、D为CH3COOCH2CH3,乙烯发生加聚反应得到F为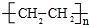 .
.
解答 解:(1)煤的干馏是再隔绝空气条件下强热,发生复杂的化学变化,
故答案为:化学;
(2)先把玻璃导管从具支试管的溶液中取出,再熄灭酒精灯,其目的是:避免具支试管中的溶液沿玻璃导管倒吸进入热的试管中,导致试管破裂,
故答案为:避免具支试管中的溶液沿玻璃导管倒吸进入热的试管中,导致试管破裂,
(3)水层有溶解的氨气,发生电离:NH3.H2O?NH4++OH-,氨水显碱性,滴加酚酞试剂,溶液显红色,苯与浓硝酸、浓硫酸在加热条件下发生取代反应生成硝基苯,反应方程式为: +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为:NH3.H2O?NH4++OH-; +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O;
+H2O;
(4)气体A与反应生成B,B可以连续氧化得到D,可知A为CH2=CH2、B为CH3CH2OH、C为CH3CHO、B为CH3COOH、D为CH3COOCH2CH3,乙烯发生加聚反应得到F为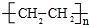 .
.
反应①的化学方程式:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,
反应④的化学方程式:CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
反应⑤的化学方程式:nCH2=CH2$\stackrel{催化剂}{→}$ ,
,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;nCH2=CH2$\stackrel{催化剂}{→}$ .
.
点评 本题考查煤的干馏、有机物推断,比较基础,旨在考查学生对基础知识的巩固,熟练掌握官能团的性质与转化.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
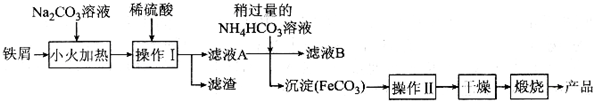
 用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g/mol)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g/mol)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 科学仪器的使用利于我们认识物质的微观世界,现在人们借助扫描隧道显微镜,应用STM技术可以“看”到越来越细微的结构,并实现对原子或分子的操纵 | |
| B. | 视频《穹顶之下》再次引起公众对“PM2.5”的关注.“PM2.5”是指大气中直径小于或等于2.5×10-6m的细小颗粒物,这些颗粒扩散在空气中形成胶体 | |
| C. | 臭氧是一种有鱼腥味、氧化性极强的淡蓝色气体,可用作自来水的消毒剂 | |
| D. | 我国油品从国 IV 汽油升级到国 V 汽油,有助于减少酸雨、雾霾,提高空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com