
下列对能量转化的认识中,不正确的是( )
A.电解水生成氢气和氧气时,电能主要转化为化学能
B.风力发电时,风能主要转化为电能
C.白炽灯工作时,电能全部转化为光能
D.煤燃烧时,化学能主要转化为热能
科目:高中化学 来源:2015-2016学年江苏省宝应县高一下学期期中调研联合考试化学试卷(解析版) 题型:选择题
下列化学用语正确的是
A.氯化钠的电子式: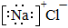 B.氯化氢的电子式
B.氯化氢的电子式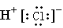
C.碳元素位于周期表中第2周期ⅥA族 D.H2O的结构式:H—O—H
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.每一周期元素都是从碱金属开始,以稀有气体结束
B.f区都是副族元素,s区和p区的都是主族元素
C.铝的第一电离能小于K的第一电离能
D.B电负性和Si相近
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高一下学期期中考试化学试卷(解析版) 题型:选择题
少量铁粉与100 mL 0.01 mol·L-1的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O②加NaOH固体③滴入几滴浓盐酸④加CuO固体⑤加NaCl溶液⑥滴加几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol·L-1的盐酸
A.①⑤⑦ B.②④⑥ C.③⑦⑧ D.③⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高一下学期期中考试化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.所有物质中都存在化学键
B.由两种元素组成的分子中一定不存在非极性共价键
C.含有离子键的化合物一定是离子化合物
D.化学键断裂的过程必发生化学反应
查看答案和解析>>
科目:高中化学 来源:2016届青海省高三下高考冲刺一理综化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质]
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式______,它位于周期表______区。
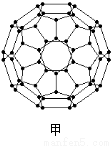
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为_______;1 mol C60分子中σ键的数目为_____个。
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As____Ga(填“>”、“<”或“=”)。
②SeO2分子的空间构型为________。
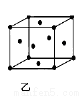
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应的化学方程式为3F2+4 NH3 Cu NF3+3 NH4F,该反应中NH3的沸点 (填“>”、“<”或“=”)HF的沸点,NH4F固体属于 晶体。往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是____________ _______ 。图乙为一个金属铜的晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2016届青海省高三下高考冲刺一理综化学试卷(解析版) 题型:选择题
X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的是
A.原子半径:W>Z>Y>X B.气态氢化物的稳定性:X<Z
C.最外层电子数:Y>W D.Y、Z的氧化物都是两性氧化物
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三模拟考试二理综化学试卷(解析版) 题型:选择题
化学与生活、能源、环境等密切相关。下列描述错误的是
A.医用酒精是用淀粉类植物发酵经蒸馏制成,浓度通常是75%
B.“雾霾天气”“温室效应”“光化学烟雾”的形成都与氮的氧化物无关
C.用CO2合成可降解的聚碳酸酯塑料,可以减少“白色污染”
D.氮化硅陶瓷是一种新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】第四周期过渡元素Mn、Fe、Ti、Ni可与C、H、O形成多种化合物。
(1)下列叙述正确的是 。(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个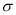 键和1个大
键和1个大 键,C6H6是非极性分子
键,C6H6是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
元 素 | Mn | Fe | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
Mn原子价电子排布式为 ,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是 。
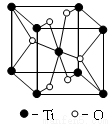
(3)根据元素原子的外围电子排布,可将元素周期表分区,其中Ti属于____________区。Ti的一种氧化物X,其晶胞结构如上图所示,则X的 化学式为 。
(4)某铁的化合物结构简式如右图所示
①组成上述化合物中各非金属元素电负性由大到小的顺序为
(用元素符号表示)
②在右图中用“→”标出亚铁离子的配位键。

(5)NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的配位数为 ,这几个O2-构成的空间构型为 。已知Ni2+与O2-的核间距为anm, NiO的摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则该晶体的密度为________ g/cm3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com