
【题目】为减小和消除过量CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
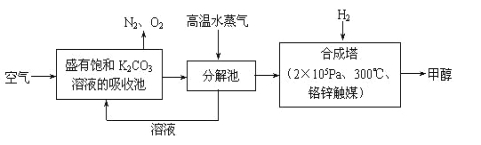
写出分解池中反应的化学方程式 。在合成塔中,当有4.4 kg CO2与足量H2完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(2)以CO2为碳源还可以制备乙醇,反应如下:
2CO2(g) + 6H2(g)=== CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol
写出由CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式 。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。当电子转移 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)以甲醇为燃料还可制作新型燃料电池,电池的正极通入O2,负极通入甲醇,用熔融金属氧化物MO作电解质(可传导O2-)。该电池负极发生的电极反应是 。
【答案】(1)2KHCO3![]() K2CO3+H2O+CO2↑(2分)
K2CO3+H2O+CO2↑(2分)
CO2(g)+3H2(g)===CH3OH(g)+H2O(g)△H=-49.47kJ/mol(2分)
(2)2CH3OH(g)===CH3CH2OH(g)+H2O(g)△H=-74.66kJ/mol(2分)
(3)①O2+2H2O+4e-===4OH-(2分)
②2CH3OH+3O2+4OH-===2CO32-+6H2O(2分);1.2mol(2分)
(4)CH3OH-6e-+3O2-===CO2+2H2O(2分)
【解析】
试题分析:(1)分解池中反应的化学方程式为2KHCO3![]() K2CO3+H2O+CO2↑;根据4.4 kg CO2与足量H2恰好完全反应,可放出4947 kJ的热量,则1 mol CO2与氢气合成甲醇放出热量49.47 kJ的热量,所以热化学方程式为CO2(g)+3H2(g)===CH3OH(g)+H2O(g) △H=-49.47kJ/mol;
K2CO3+H2O+CO2↑;根据4.4 kg CO2与足量H2恰好完全反应,可放出4947 kJ的热量,则1 mol CO2与氢气合成甲醇放出热量49.47 kJ的热量,所以热化学方程式为CO2(g)+3H2(g)===CH3OH(g)+H2O(g) △H=-49.47kJ/mol;
(2)2CO2(g) + 6H2(g)=== CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol,根据盖斯定律,对(1)中方程式乘以2然后用该方程式减去(1),可以得到CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式为2CH3OH(g) ===CH3CH2OH(g)+ H2O(g) △H=-74.66kJ/mol。
(3)①在甲醇燃料电池中,氧气在正极上被还原,在碱性条件下生成水,电池正极电极反应式为 O2 +2H2O+4e-=== 4OH-。
②工作一段时间后,测得溶液的pH减小,则该电池总反应的化学方程式为2CH3OH + 3O2 + 4OH- === 2CO32- + 6H2O。参加反应的氧气的体积是6.72L(标准状况下),物质的量是0.3mol,转移电子物质的量为1.2mol。
(4)甲醇在负极失去电子,该电池负极发生的电极反应是CH3OH-6e-+3O2-=== CO2+2H2O。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】下列对分子或离子的立体构型判断不正确的是 ( )。
A.NH4+和CH4都是正四面体形
B.CO2和CS2都是直线形
C.NCl3和BCl3都是三角锥形
D.H2O和H2S都是V形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫物质燃烧会产生大量烟气,主要成分是SO2、CO2、N2和O2。某研究性学习小组在实验室利用下列装置制备模拟烟气,并测算模拟烟气通过转化器的脱硫效率。
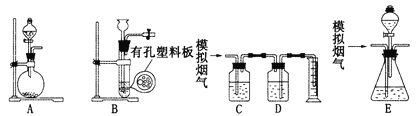
回答下列问题:
I.模拟烟气的制备
(1)用A装置制SO2的化学方程式为______________________________。
(2)用B装置制CO2,使用该装置的优点是___________________________。
(3)将制得的气体与空气充分混合,获得模拟烟气用于后续实验。
Ⅱ.测定烟气中SO2的体积分数
(4)将部分模拟烟气缓慢通过C、D装置,C、D中盛放的药品分别是____、____(填序号):
①KMnO4溶液②饱和NaHSO3溶液③饱和Na2CO3溶液④饱和NaHCO3溶液
(5)若模拟烟气的流速为a mL·min-1,t1 min后,测得量筒内液体的体积为V mL则SO2的体积分数是_______________(写表达式)。
III.测算模拟烟气通过转化器的脱硫效率(已转化的SO2占原有SO2的百分比)
(6)将模拟烟气通过转化器E装置,E装置中盛有FeC12和FeCl3的混合溶液,常温下,它可催化SO2与O2的反应,以达到脱硫的目的。写出催化剂参与反应过程的离子方程式:
①SO2+2H2O+2Fe3+==SO42-+2Fe2++4H+;②______________________________。
(7)若模拟烟气仍以a mL· min-1的流速直接通过转化器E装置,t2 min后,向E装置中加入足量的盐酸酸化的BaCl2溶液得到白色浑浊液,经_______、 洗涤、_____、称量,得到m g固体。若实验的气体体积已折算为标准状况,则该转化器的脱硫效率是_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知咖啡酸的结构如图所示。关于咖啡酸的描述正确的是:(______)
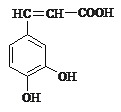
A.分子式为C9H5O4
B.1 mol 咖啡酸最多可与5 mol 氢气发生加成反应
C.与溴水既能发生取代反应,又能发生加成反应
D.1 mol 咖啡酸最多可与3 mol Na2CO3发生反应
(2)A、B、C、D1、D2、E、F、G、H均为有机化合物,请根据下列图示回答问题。
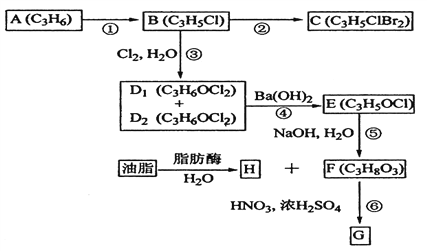
(1)直链有机化合物A的结构简式是__________________;
(2)B中官能团的名称为___________,H中含氧官能团的结构简式为____________;
(3)①的反应试剂和反应条件是___________________,③的反应类型是_____________;
(4)B生成C的化学方程式是___________________;
D1或D2生成E的化学方程式是___________________;
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有两瓶失去标签的溶液,其中一瓶是K2SO4溶液,另一瓶是NaOH溶液.鉴别时,下列选用的试纸或试剂不正确的是( )
A.pH试纸
B.紫色石蕊试液
C.Na2CO3固体
D.CuCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知一氧化碳与水蒸气的反应为: CO(g) + H2O(g)![]() CO2(g) + H2(g)
CO2(g) + H2(g)
在427 ℃ 时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0. 01 mol/L,则一氧化碳在此反应条件下的转化率为___________。
(2)规律是对经常出现的客观现象的归纳。规律越普遍,适用性或预言性也就越强,然而,任何规律都有其适用范围。
① 某同学在实验中发现,将H2S气体通入CuSO4溶液中,生成了黑色沉淀。请写出反应的化学方程式 ____________。
② 酸性强弱除与物质的本性有关外,还与溶剂有关,如CH3COOH与HF在液氨中可完全电离。在液氨中,反应CH3COONa + HCl = NaCl + CH3COOH _______(填“能”或“不能”)发生,理由是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于元素周期表,下列叙述中不正确的是( )。
A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B.在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素
C.在金属元素区域可以寻找制备新型农药材料的元素
D.周期表中位置靠近的元素性质相近
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:Na>MgO>SiO2
B.水溶性:SO2>H2S>HCl
C.热稳定性:HF>H2O>NH3
D.沸点:HF>HCl>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是常见的氧化剂、催化剂和活性电极材料。
(1)工业上,以惰性材料为电极,电解MaSO4溶液(含少量稀硫酸)制备MnO2。写出阳极的电极反应式:_________________________________。
(2)已知如下热化学方程式(K代表平衡常数):
①MnCO3(s)![]() Mn0(s)+CO2(g)△H1 K1
Mn0(s)+CO2(g)△H1 K1
②2MnO(s)+O2(g)![]() 2MnO2(s)△H2 K2
2MnO2(s)△H2 K2
③2MnCO3(n)+O2(g)![]() 2MnO2(s)+2CO2(g)△H3 K3
2MnO2(s)+2CO2(g)△H3 K3
△H3=________用△H1,△H2表示);K3=________用K1、K2表示)。
(3)反应②在低温条件下能自发进行,则△H3________0(填“>"“<"或“=")。
(4)在密闭容器中投入足量的MnCO3,一定条件下发生反应MnCO3(s)![]() MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
①温度、压强对MnCO3分解率的影响如图所示:
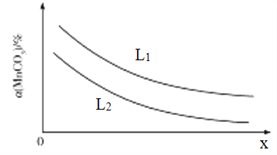
比较:L1__________L2(填“>"“<”或“=")。
②保持温度不变,将容器休积扩大至原来的2倍,则ρ(CO2)的变化范围是____________。
③保持温度不变,将容器体积压缩至原来的一半,达到新平衡时下列物理量一定不变的是____(填代号)。
A.平衡常数K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)一定温度下,在容积为2L的恒容密闭容器中加入足量的MnCO3(s)和5molO2,发生反应:2MnCO3(s)+O2(g)![]() 2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com