
| A. | X中阳离子和阴离子个数一定相等 | |
| B. | X中可能既含离子键,又含共价键 | |
| C. | 若X只含两种元素,则两种元素可在同一周期也可在同一主族 | |
| D. | X中阳离子半径一定大于阴离子半径 |
分析 由短周期元素构成的某离子化合物X中,一个阳离子和一个阴离子核外电子数之和为20.阴、阳离子均是10电子微粒,它们可以是:阴离子:N3-、O2-、F-、OH-等,阳离子:NH4+、Na+、Mg2+、Al3+等,据此判断.
解答 解:由题意知阴、阳离子均是10电子微粒,它们可以是:阴离子:N3-、O2-、F-、OH-等,阳离子:NH4+、Na+、Mg2+、Al3+等.
A.当阴、阳离子所电荷相等,阳离子和阴离子个数相等,如NaF、NaOH,当阴、阳离子所电荷不相等,阳离子和阴离子个数不相等,如MgF2、Na2O,故A错误;
B.X是离子化合物,一定有离子键,也可能含共价键,如NaOH、Mg(OH)2、NH4F等,故B正确;
C.若X只含两种元素可以是NaF、MgF2、Na2O、Na3N等,两元素不能在同一周期也不能在同一主族,故C错误;
D.对简单的离子,阴、阳离子电子层结构相同,核电荷数越大,离子半径越小,阳离子的核电荷数一定大于阴离子的核电荷数,所以X中阳离子半径小于阴离子半径,故D错误.
故选:B.
点评 本题考查离子结构、物质结构等知识,难度中等,本题采取列举法解答,找出例外举例,列举法在元素周期表中经常利用.


科目:高中化学 来源: 题型:解答题
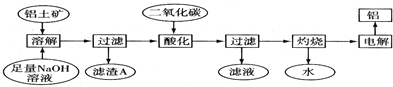
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 溶液变(血)红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入1~2滴③或④(填序号)溶液,振荡 | 紫红色褪去或产生蓝色沉淀 | 存在Fe2+ |
| 实验编号 | 操 作 | 现 象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无水硫酸 | B. | 无水氯化钙 | C. | 生石灰 | D. | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若R(OH)n为强碱,则W(OH)n+1也为强碱 | |
| B. | 若最高氧化物的水化物HnXOm为强酸,则Y是活泼非金属元素 | |
| C. | 若Y的最低化合价为-2,则Z的最高正化合价为+6 | |
| D. | 若X的最高正化合价为+5,则五种元素都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
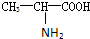 ),苯丙氨酸(
),苯丙氨酸(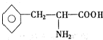 )
)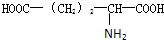 ),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )
),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )| A. | 10,4,3 | B. | 10,3,4 | C. | 9,4,3 | D. | 9,3,4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
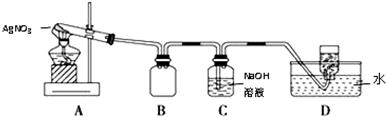
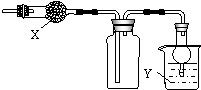 如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )| 选项 | X | 收集气体 | Y |
| A | 碱石灰 | 氯化氢 | 水 |
| B | 碱石灰 | 氨气 | 水 |
| C | 氯化钙 | 二氧化硫 | 氢氧化钠溶液 |
| D | 氯化钙 | 一氧化氮 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 假若为平面四边形,则有三种同分异构体 | |
| B. | 假若为四面体,则有两种同分异构体 | |
| C. | 假若为平面四边形,则无同分异构体 | |
| D. | 假若为四面体,则无同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com