
【题目】(1)质量比为16∶7∶6的三种气体SO2、CO、NO,分子个数之比为_____________;氧原子个数之比为____________。
(2)在标准状况下,6.8g PH3与标准状况下_______L CH4含有相同数目的H原子。
(3)某气体氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为________,R的相对原子质量为________。
(4)273 K、1.01×105 Pa时气态单质X2的密度为1.25 g·L-1,则X的相对原子质量为________
(5)相同温度和压强条件下,一定体积的气态氢化物H2R的质量是等体积NH3的2倍,则R的相对原子质量为____________。
【答案】5:5:4 10:5:4 3.36 64g.mol-1 32 14 32
【解析】
(1)根据n=![]() 计算SO2、CO、NO的物质的量之比,分子数目之比等于其物质的量之比,结合分子式计算含有氧原子数目之比;
计算SO2、CO、NO的物质的量之比,分子数目之比等于其物质的量之比,结合分子式计算含有氧原子数目之比;
(2)依据n=![]() =
=![]() =
=![]() ,结合PH3含有3个H,CH4含有4个H解答;
,结合PH3含有3个H,CH4含有4个H解答;
(3)根据n=![]() 计算RO2的物质的量,再根据M=
计算RO2的物质的量,再根据M=![]() 计算其摩尔质量,进而计算R的相对原子质量;
计算其摩尔质量,进而计算R的相对原子质量;
(4)依据ρ标=![]() 计算M,然后计算X的相对原子质量;
计算M,然后计算X的相对原子质量;
(5)相同状态下,气体摩尔体积相等,相同体积的不同气体其物质的量相等,根据m=nM计算X的摩尔质量。
(1)质量比为16∶7∶6的三种气体 SO2、CO、NO物质的量之比为![]() ∶
∶![]() ∶
∶![]() =5∶5∶4,故三者分子数目之比为5∶5∶4,含有氧原子数目之比为5×2∶5×1∶4×1=10∶5∶4,故答案为:5∶5∶4;10∶5∶4;
=5∶5∶4,故三者分子数目之比为5∶5∶4,含有氧原子数目之比为5×2∶5×1∶4×1=10∶5∶4,故答案为:5∶5∶4;10∶5∶4;
(2)依据n=![]() =
=![]() =
=![]() ,要使二者含有氢原子数相等则满足:
,要使二者含有氢原子数相等则满足:![]() ×3=
×3=![]() ×4,解得V=3.36L,故答案为:3.36;
×4,解得V=3.36L,故答案为:3.36;
(3)RO2的物质的量为![]() =0.02mol,其摩尔质量为
=0.02mol,其摩尔质量为![]() =64g/mol,R的相对原子质量为64-32=32,故答案为:64g/mol;32;
=64g/mol,R的相对原子质量为64-32=32,故答案为:64g/mol;32;
(4)273K、1.01×105Pa时气态单质X2的密度为1.25gL-1,则M=ρ标×22.4L/mol=1.25gL-1×22.4L/mol=28g/mol;则X的相对原子质量为![]() =14,故答案为:14;
=14,故答案为:14;
(5)相同状态下,气体摩尔体积相等,相同体积的不同气体其物质量相等,根据m=nM知,相同物质的量时气体质量与摩尔质量成正比,相同状况下,一定体积的气态氢化物H2R的质量是等体积NH3的2倍,则H2R的摩尔质量是氨气的2倍,为34g/mol,则R摩尔质量=(34-2)g/mol=32g/mol,相对原子质量为32,故答案为:32。


科目:高中化学 来源: 题型:
【题目】已知某“84”消毒液瓶体部分标签如图所示,该“84 消毒液通常稀释100 倍(体积之比)后使用。请回答下列问题:

(1)“84消毒液的物质的量浓度约为_______(保留一位小数molL-1)
(2)某同学取20mL该“84"消毒液,稀释后用于消毒,稀释后的溶液中c(Na+)=______mol
(3)“84”消毒液与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8gcm-3)的浓硫酸配制1L3.6mo1L-1稀硫酸用于增强“84”消毒液的消毒能力。需用浓硫酸的体积为______mL;配制该溶液需要的仪器有玻璃棒、烧杯、量筒和_______(填玻璃仪器名称)
(4)若配制3.6mol/L的硫酸溶液的其他操作均正确,但出现下列错误操作,将使 所配制的硫酸溶液浓度偏低的是_______(填字母代号,多选题,少选不给分)
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.稀释过程中,溶液未经冷却就转移至容量瓶
C.所用浓硫酸长时间放置在密封不好的容器中
D.用胶头滴管向容量瓶中加水时,俯视观察溶液凹液面与容量瓶刻度相切
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中发生反应2SiHCl3(g)SiH2Cl2(g)+SiCl4(g)。在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。下列说法正确的是( )

A. 323 K时,缩小容器体积可提高SiHCl3的转化率
B. a、b点对应的反应速率大小关系:v(a)<v(b)
C. 343 K时,上述反应的化学平衡常数约为0.02
D. 2SiHCl3(g)SiH2Cl2(g)+SiCl4(g)的正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用盐酸的质量分数为36.5%,密度为1.20 g·mL-1。
(1)此浓盐酸中HCl的物质的量浓度是________。
(2)配制100 mL该浓盐酸,需要标准状况下HCl的体积为________。
(3)配制100 mL 3.00 mol·L-1的盐酸,需以上浓盐酸的体积为________。
(4)将10.0 mL 3.00 mol·L-1的盐酸与10.0 mL 1.00 mol·L-1的MgCl2溶液混合,则混合溶液中Cl-的物质的量浓度是________。(设混合后溶液的体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2加氢合成甲醇是合理利用CO2的有效途径。由CO2制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH1=+41.19 kJ·mol-1
CO(g)+H2O(g) ΔH1=+41.19 kJ·mol-1
反应Ⅱ:CO(g)+2H2(g) ![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
反应Ⅲ:CO2(g)+3H2g) ![]() CH3OH(g)+H2O(g) ΔH3=-49.58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH3=-49.58 kJ·mol-1
回答下列问题:
(1)反应Ⅰ、Ⅱ、Ⅲ的化学平衡常数分别为K1、K2、K3、则K3=__________(用K的代数式表示)
(2)在恒压密闭容器中,充入一定量的 H2 和 CO2(假定仅发生反应Ⅲ),实验测得反应物在不同温度下,反应体系中 CO2 的平衡转化率与压强的关系曲线如图 1 所示。

①比较 T1 与 T2 的大小关系:T1____________T2(填“<”、“=”或“>”)
②在 T1 和 p6 的条件下,往密闭容器中充入 3 mol H2 和 1 mol CO2,该反应在第 5 min 时达到平衡,此时容器的体积为 1.8 L,则该反应在此温度下的平衡常数为________。
a.若此条件下反应至 3 min 时刻,改变条件并于 A 点处达到平衡,CH3OH 的浓度随反应时间的变化趋势如图 2所示(3~4 min 的浓度变化未表示出来),则改变的条件为 __________,请用 H2 的浓度变化计算从4 min开始到 A点的反应速率v(H2)= _________(保留两位小数)。
b.若温度不变,压强恒定在 p8 的条件下重新达到平衡时,容器的体积变为_______L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于非氧化还原反应的是( )
A. Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
B. NH4NO3![]() N2O↑十2H2O
N2O↑十2H2O
C. 2FeCl2+Cl2=2FeCl3
D. Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应:N2(g)+O2(g)![]() 2NO(g)ΔH >0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
2NO(g)ΔH >0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
(1)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.5 mol,则N2的反应速率为_____________________。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志________ 。
A.消耗1 mol N2同时生成1 mol O2
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.2v正(N2)=v逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下图变化趋势正确的是____________(填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数________。(填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mol·L-1、4.0×10-2 mol·L-1和3.0×10-3 mol·L-1,此时反应___________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
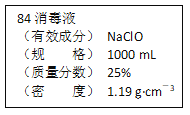
(1)该“84消毒液”的物质的量浓度约为_____mol·L-1。
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是________(填字母)。
A.溶液中NaClO的物质的量 B.溶液的浓度
C.溶液中NaClO的摩尔质量 D.溶液的密度
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。回答下列问题。
①如图所示的仪器中,有些是不需要,配制上述溶液还需要玻璃仪器_______

②需要称量NaClO固体的质量为_______ g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制200 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________mol·L-1。
②需用浓硫酸的体积为________ mL。
③若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_______。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻。已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸。
(1)D元素基态原子的外围电子排布式为____________________。
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为________________(用相应的元素符号作答)。
(3)B、X、D氢化物的沸点由高到低的顺序为_______________(用相应的化学式作答)。
(4)C元素的原子可形成多种离子,试推测下列微粒的立体构型(C为字母,不是碳元素):
微粒 | CO32- | CO42- |
立体构型名称 | _______________ | _______________ |
(5)元素B的一种氢化物B2H4具有重要的用途。有关B2H4的说法正确的是_______。
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)E元素和D元素在同一周期,属于VIII族,价层有三个单电子,E(OH)2为两性氢氧化物,在浓的强碱溶液中可形成E(OH)42-,写出E(OH)2酸式电离的电离方程式___________________。
(7)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如图所示)中F原子的配位数之比为___________,δ、γ、α三种晶胞的边长之比为_____________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com